 Все авторефераты докторских диссертаций
Все авторефераты докторских диссертаций
Промышленные технологии производства биологически активных веществ из сырья природного происхождения
Автореферат докторской диссертации
На правах рукописи
ФРОЛОВА
МАРИНА АЛЕКСЕЕВНА
ПРОМЫШЛЕННЫЕ ТЕХНОЛОГИИ ПРОИЗВОДСТВА БИОЛОГИЧЕСКИ АКТИВНЫХ ВЕЩЕСТВ ИЗ СЫРЬЯ ПРИРОДНОГО ПРОИСХОЖДЕНИЯ
03.01.06 - биотехнология (в том числе бионанотехнологии)
АВТОРЕФЕРАТ
диссертации на соискание ученой степени
доктора биологических наук
Щелково - 2012
Работа выполнена в ГНУ Всероссийский научно-исследовательский и технологический институт биологической промышленности Российской академии сельскохозяйственных наук
Научный консультант: академик РАСХН, академик НААН Украины, доктор ветеринарных наук, профессор, лауреат Государственной премии РФ, Заслуженный деятель науки РФ Самуйленко Анатолий Яковлевич
Официальные оппоненты:
Мелентьев Александр Иванович-доктор биологических наук, профессор, Институт биологии УН - РАН, директор;
Скотникова Татьяна Анатольевна-доктор биологических наук, ГНУ Всероссийский научно-исследовательский и технологический институт биологической промышленности, зав. лабораторией обеспечения качества вакцин;
Балышева Вера Ивановна-доктор биологических наук, ГНУ Всероссийский научно-исследовательский институт ветеринарной вирусологи и микробиологии, ведущий научный сотрудник лаборатории биотехнологии.
Ведущая организация: ГНУ Всероссийский научно-исследовательский институт экспериментальной ветеринарии им. Я.Р. Коваленко
Защита состоится 29 июня 2012 года в 10 часов на заседании диссертационного совета Д 006.069.01 по защите диссертаций на соискание ученой степени доктора наук при Всероссийском научно-исследовательском и технологическом институте биологической промышленности РАСХН по адресу: 141142, Московская область, Щелковский район, пос. Биокомбината, д.17, ВНИТИБП, e-mail:
С диссертацией можно ознакомиться в библиотеке Всероссийского научно-исследовательского и технологического института биологической промышленности.
Автореферат разослана л ____________ 2012 г.
Ученый секретарь диссертационного совета,
кандидат биологических наукаа Фролов Юрий Дмитриевич
1.ОБЩАЯ ХАРАКТЕРИСТИКА РАБОТЫ
1.1.Актуальность работы. Разработка промышленной технологии производства биологически активных веществ из сырья природного происхождения является важной задачей биотехнологии, позволяющей осуществить более полное и комплексное использование биоресурсов.
В настоящее время вопросами разработки препаратов на основе переработки морепродуктов в различных областях народного хозяйстваа занимаются многие научные коллективы как в нашей стране, так и за рубежом (Новикова М.В. с соавт., 1997; Самуйленко А.Я. с соавт.,2003; Быкова В.М. с соавт.,2003; Гамзазаде А.И. с соавт.,2003; Большаков И.Н. с соавт.,2003; Фомичев Ю.П. с соавт., 2006; Wall D. et al., 2001; Chaidedgumjorn et al., 2002; Muzzarelli R.A.A. et al., 2005).
Хитозан привлекает внимание широкого круга исследователей и практиков благодаря комплексу афизико-химических и биологических свойств и неограниченной воспроизводимой сырьевой базе. Полисахаридная природа хитозана обусловливает его сродство к живым организмам, а наличие реакционноспособных функциональных групп обеспечивает возможность разнообразных химических модификаций, позволяющих усиливать присущие ему свойства или придавать новые в соответствии с предъявленными требованиями.
Значительный вклад в изучение хитина и хитозана внесли ученые: Быков В.П.,а Рогожин С.В., Гамзазаде А.И., В.П., Варламов В.П., Албулов А.И.,аа Немцев С.В., Нудьга Л.А., Скрябин К.Г., Сафронова Т.М., Быкова В.М., Вихорева Г.А., Феофилова Е.П., Маслова Г.В., Новиков В.Ю.,а Куприна Е.Э., Михайлов С.Н., Кильдеева Н.Р., Липатова И.М., Александрова В.А., Комаров Б.А., Марквичева Е.А., Урьяш В.Ф., Братская С.Ю., Тихонов В.Е., Лопатин С.А., Велешко А.Н., Ежова Е.А., Акопова Т.А и другие исследователи, работы которых направлены на изучение свойств хитина и хитозана, способов их получения аиз разных видов сырья и применения в различных областях народного хозяйства.
Производство ферментных препаратов является одним из перспективных направлений в современной биотехнологии. Ежегодный мировой прирост объема их производства в настоящее время составляет 10-15 %. Наибольший удельный вес среди выпускаемых ферментных препаратов (до 60% общего объема)а занимают протеиназы и амилазы. В настоящее время отечественная промышленность заметно отстает по объему производства ферментов от ведущих зарубежных стран, а высокие цены на коммерческие трипсины зарубежных производителей стимулируют интерес к разработке и усовершенствованию технологических процессов его получения.
Применяемые в настоящее время методы выделенияа ДНК из сырья животного происхождения многостадийны, трудоемки и требуют дорогостоящего оборудования и реактивов. У нас в стране и за рубежом она производится в небольших объемах. Основным недостатком большинства способов получения ДНК является дороговизна и сложность их воспроизведения в промышленных условиях. В связи с этим, разработка промышленной технологии получения дезоксирибонуклеиновой кислоты для практического примененияа актуальна.
Одним из современных подходов к решению проблемы иммунной недостаточности у молодняка сельскохозяйственных животных является разработка, производство и применение новых экологически безопасных эффективных препаратов, таких как пробиотики и пребиотики,а которые в малых амалых дозах способны существенно изменять обмен веществ и повышать общую резистентность организма (Панин А.Н., 1997; Субботин В.В. с соавт.,1998; Тараканов Б.В., 1998; 2002; Малик Н.И., 2002; Архипов А.В., 2010).
Богатейший источник биологически активных веществ - обитатели Мирового океана, в частности моллюски, в мясе которых обнаружены соединения, обладающие широким спектром биологической и фармакологической активности. Способность повышать общую резистентность организма связывают с наличием в мидийных препаратах липидных антиоксидантов, меланоидинов и микроэлементов.
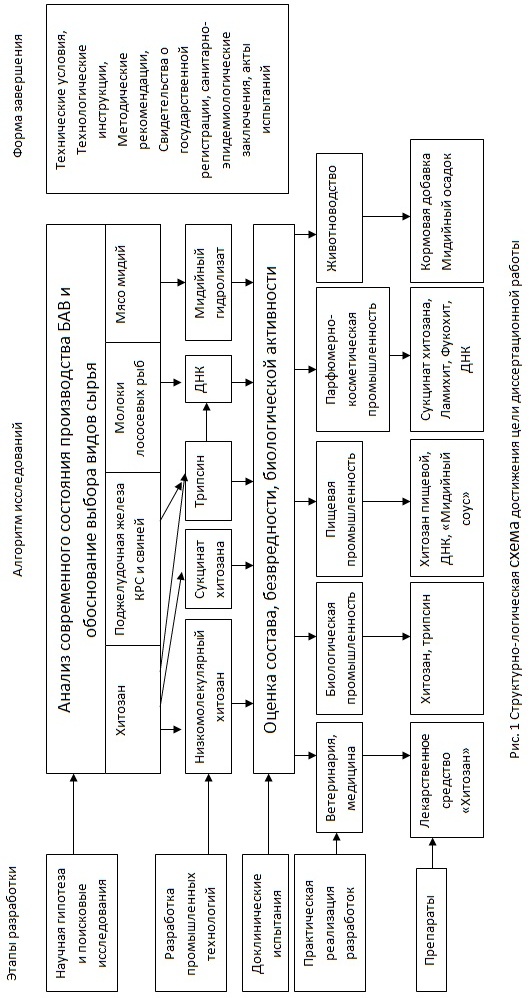
аа 1.2. Цель и задачи исследований. Цельа работы - разработка промышленных технологий изготовления биологическиа активных веществ из сырья природного происхождения и создание на их основе новых экологически безопасных эффективных биопрепаратов для применения в различных отраслях народного хозяйства.
Для достижения поставленной цели были определены следующие задачи:
- проанализировать современное состояние производства биологически активных веществ;
-разработать технологические процессы производства производных хитозана, протеолитического ферментного препарата трипсина, дезоксирибонуклеиновой кислоты и мидийного гидролизата;
-изготовить опытные образцы препаратов,а изучить их физико-химические свойства,а биологическую активность и эффективность применения в различных отраслях народного хозяйства;
- разработать нормативную документацию на препараты и освоить их промышленный выпуск.
аа 1.3. Научная новизна. Впервые разработаны промышленные технологии получения ахитозанаа с заданными характеристиками адля практического применения.
Установленаа профилактическая и терапевтическая эффективность низкомолекулярного хитозана (ММ 5-10 кДа) при гамма-облучении мышей радиоцезием в летальных дозах.
Научно обоснована и экспериментально доказана целесообразность использования хитозана для терапии и профилактики желудочно-кишечных заболеваний молодняка сельскохозяйственных животных.
Показана высокая ростостимулирующая активность хитозана при введении его в рацион подсосным свиноматкам и поросятам, при этом у животных отсутствовала стрессорная реакция адаптационного синдрома.
Установлены высокие сорбционные свойства хитозана в отношении бактерий аP.multocida и показана возможность его использования в качестве флокулянта в технологическом процессе концентрирования бакмассы.
Научно обоснованаа и экспериментально доказана эффективность влиянияа комплекса пробиотика Провагена с хитозаном на микробиоценоз толстого кишечника, динамику живой массы и морфо-биохимические показатели гомеостаза телят.
Экспериментально доказана эффективность выпаивания раствора хитозана из расчета 5 мг/головуа начиная с 32-х дневного возраста в составе рациона кормления на среднесуточный прирост и живую массу цыплят-бройлеров.
Включение в рецептуруа лечебно-профилактической зубной пасты низкомолекулярного водорастворимого хитозана (ММ 10-40 кДа) позволило получить пасту с противовоспалительным и кариеспрофилактическим действием, а также высокими очищающими и дезодорирующими свойствами (Патент РФ № 2328267).
Впервые разработана промышленная технология изготовления протеолитического ферментного препарата трипсина, отличающаяся экологической безопасностьюа производства, с применением адсорбента -а природного полисахарида хитозана а(Патент РФ № 2265053; Патент РФ № 2437936).
Впервые разработана промышленная технология изготовления дезоксирибонуклеиновой кислоты (ДНК) из молок лососевых рыб с использованием ферментного препарата трипсина.
Впервые разработана экологически безопасная апромышленная технология получения Мидийного гидролизатаЦбиологически активной пищевой добавки из мяса мидийа Мидийный соус. (Патент РФ № 2284708).
Экспериментально обоснованы схемы применения Мидийного препарата при выращивании молодняка сельскохозяйственных животных и птицы для увеличения интенсивности роста и уровня естественной резистентности.
а 1.4. Практическая значимость работы
Результаты исследований использованы при разработке технологий изготовления: различных форм и модификаций хитозана (Хитозана пищевой; лекарственного средства для лечения и профилактики желудочно-кишечных заболеваний молодняка сельскохозяйственных животных Хитозан; косметического сырья Сукцинат хитозана, Ламихит - экстракта ламинарии с хитозаном, Фукохит - экстракта фукуса с хитозаном); протеолитического ферментного препарата трипсина; дезоксирибонуклеиновой кислоты из молок лососевых; мидийного гидролизата - биологически активной пищевой добавки из мяса мидийа Мидийный соус.
Промышленный выпуск разработанных препаратов освоен на производственном участке отдела получения биологически активных веществ ВНИТИБП и в ЗАО Биопрогресс.
Создание новых технологий и организацияа промышленного выпуска биологически активных веществ дали возможность их применения:
- в ветеринарииа (лекарственное средство Хитозан);
- в пищевой промышленности (Хитозан пищевой, биологически активная добавка Кислота дезоксирибонуклеиновая из молок лососевых рыб, биологически активная пищевая добавка Мидийный соус);
- в биологической промышленности (ферментный препарат трипсин);
- в парфюмерно-косметической промышленности (косметическое сырье Сукцинат хитозана, Ламихит, Фукохит, Кислота дезоксирибонуклеиновая из молок лососевых рыб).
Годовой объем выпуска биологически активных веществ в зависимости от вида продукции и потребностейа составляет от 800 кг до 3-5 тонн.
аа 1.5 Основные положения диссертации, выносимые на защиту:
-промышленные технологии изготовления низкомолекулярного хитозана и сукцината хитозана;
-параметры острой и хронической токсичности хитозана;
-радиопротекторные и флоккулирующие свойства хитозана;
- различные формы хитозана в ветеринарной практике;
-оценка эффективности влияния препаратов хитозана на резистентность сельскохозяйственных животных и птицы;
-хитозан в составе кормовых добавока для сельскохозяйственных животных и птицы;
-хитозан в технологии получения протеолитического ферментного препарата трипсина;
-хитозан в составе парфюмерно-косметической апродукции;
-промышленная технология изготовления дезоксирибонуклеиновой кислоты (ДНК) и практические аспекты ее применения;
-промышленная технология получения Мидийного гидролизата;
-эффективность применения мидийного гидролизата для повышения резистентности молодняка сельскохозяйственных животных и птицы.
1.6. Апробация работы. Основные материалы доложены и обсуждены:
- в виде ежегодных отчетов по темам госзаданий на заседаниях ученого совета и методических комиссий ВНИТИБП (1996-2011 гг.); на секции Ветеринарная биотехнология Отделения ветеринарной медицины Россельхозакадемии (2008-2011 гг.); наа Международных конгрессах в Москве, Санкт-Петербурге, Минске, Ялте, Алуште,Харькове, Всесоюзных, Республиканских и Всероссийских конференциях в Москве, Санкт-Петербурге, Орле, Черноголовке, Щелково, Ставрополе, Казани, Пущино, Махачкале, Луганске, Светлогорске, Нижнем Новгороде, Ярославле, Воронеже, Боровске, Южно-Сахалинске, Уфе, Армавире, Краснодаре (1996-2012 гг.).
Разработкиа демонстрировались на выставках:а II Международная выставка Инновации 99. Технологии живых систем (Москва, 1999); аVIII выставка Медицина для Вас (Москва, 2001);а Международная выставка Биотехника (Ганновер, 2001); аII Международная выставка Планета и здоровье (Москва, 2001); Биотехнологии России (Берлин, 2001); Лаборатория-Экспо (Москва, 2009-2011);а Биоиндустрия-биотехнологические решения для здравоохранения (С.-Петербург, 2011); Российская агропромышленная выставка Золотая осень (Москва, 2002-2011 гг.). Разработки по материалам диссертационной работы были награжденыа 16 дипломами, 7 золотыми, 3 серебряными и 1 бронзовой медалью ВДНХ СССР и ВВЦ. За разработку промышленных технологий изготовления биологически активных препаратов и внедрение их в производство авторома получены 4 медали Лауреат ВВ - и серебряная медаль РАЕН имени Е. Дашковой.
аа 1.7. Публикации. Основные положения диссертационной работы опубликованы в 101 научной работе, в том числе в 1 монографии и 19 статьях в изданиях по перечню, рекомендованному ВАК Минобрнауки России. По материалам исследований получено 4 Патента РФ на изобретения.
аа 1.8. Объем и структура диссертации. Диссертация изложена на 324 страницах и состоит из введения, обзора литературы, собственных исследований, включающих материалы и методы, результаты, выводы и практические предложения, содержит 42 таблицы и 33 рисунка. Список литературы включает 442 наименования, из которых 299 отечественных и 143 зарубежных. В приложении представлены копии документов, подтверждающие достоверность работы, ее научную и практическую значимость.
аа 1.9. Личный вклад автора заключается в формулировании проблемы, постановке целей и задач исследований, теоретическом и методическом обосновании путей решения поставленных задач, непосредственном планировании экспериментов и выполнении исследований, обобщении и интерпретации результатов, разработке нормативной документации, организации апробации и промышленного производства разработанных препаратов.
аа 1.10. Благодарности. Автор выражает благодарность научному консультанту директору ВНИТИБП, академику РАСХН А.Я.Самуйленко. За практическую и консультативную помощь выражаю благодарность заведующему отделом получения БАВ ВНИТИБП доктору биологических наук, профессору аА.И. Албулову, сотрудникам института А.С.Фоменко, С.М. Шинкареву В.И. Еремцу, Л.А.Неминущей, Т.А.Скотниковой, Т.А.Авдеевой, В.Н.Кача-лову, а также сотрудникам Центра Бионженерия РАН В.П.Варламову, С.А.Лопатину, Брянской ГСХА Е.В.Крапивиной, Старовойтовой Р.П., ВНИРО С.В.Немцеву, ИПХФ Б.А.Комарову, Уральской ГАВМ А.Р.Таировой, Белорусской ГСХА П.А.Красочко, МГАВМиБ им. К.И.Скрябина, ВГНКИ, ВНИИВВиМ, ФГУП Щелковский биокомбинат.
2. Материалы и методы
Работа выполнена в 1996-2012 гг. во ВНИТИБП согласно планам НИР и ОКР, а также в плане реализации творческого научного сотрудничества Брянской ГСХА и ГНУ ВНИТИБП в объеме комплексных исследований по темеа Изучение иммунного статуса и разработка мероприятий повышения резистентности свиней Брянской области и Договора о творческом сотрудничестве Национального университета биоресурсов и природоиспользования (НУБиП) Украины (г. Киев) иа ГНУ ВНИТИБП по проведению совместных исследований по вопросам создания, изучения и применения препаратов на основе хитозана в сфере ветеринарной медицины и животноводства.
Экспериментальные исследования осуществляли в отделе получения БАВ ВНИТИБП, ЗАО Биопрогресс, Центре Биоинженерия РАН,а Брянской ГСХА, УО Белорусская государственная сельскохозяйственная академия, РУП Институт экспериментальной ветеринарии имени С.Н.Вышелесского Республики Беларусь, Уральской государственной академии ветеринарной медицины, Казанском НИИ эпидемиологии и микробиологии, в хозяйствах Московской, Тульской и Брянской областей (Агрофирма Повадинская, СХПК Заря Подмосковья и Щелковская птицефабрика Московской области, АОЗТ Красное и КСХП Приупское Тульской области,а СТФ СПК Родина, ОУХ Кокино и СТФ СПК Культура Брянской области).
Эффективность разработок испытывали в ЗАО Биопрогресс,а ФГУП Ставропольская биофабрика, ФГУП Армавирская биофабрика, ОАО Покровский завод биопрепаратов.
Объектами исследований служили опытно-промышленные партии хитозана с различной молекулярной массой (80 кДа, 150 кДа, 300 кДа, 380 кДа, 500 кДа) и растворимостью (кислоторастворимый и водорастворимый); опытно-промышленные партииа ферментного препарата трипсина; опытно-промышленные партии препарата дезоксирибонуклеиновой кислоты (ДНК); опытно-промышленные партии мидийного препарата.
аа Животные: телята черно-пестрой породы 2 - 8-суточного возраста и 1Ц1,5-месячного возраста для оценки эффективности применения препаратов хитозана для лечения и профилактики желудочно-кишечных заболеваний у молодняка сельскохозяйственных животных и изучения влияния апробиотика Проваген и комплекса этого пробиотика с хитозаном на микробиоценоз толстого кишечника, динамику живой массы и морфо-биохимические показатели гомеостаза телят;апоросята крупной белой породы (сосуны и отъемыши), подсвинки крупной белой породы 3,5-4,5-месячного возраста, свиноматки крупной белой породы для оценки эффективности применения препаратов хитозана для лечения и профилактики желудочно-кишечных заболеваний у молодняка сельскохозяйственных животных и изучения влияния Мидийного препарата на резистентность сельскохозяйственных животных;ацыплята-бройлеры кросса Гибро и цыплята породы кросс П-46 18-суточного и 6-суточного возраста для оценки эффективности применения Мидийного препарата;белые беспородные мыши-самцы массой 18-20 г, 25 г и 25-30 г для оценки токсичности препаратов.
аМатериалы и методы: хитин из панцирей камчатских крабов (ТУ 15-01-472) - для изготовления хитозана:аподжелудочная железа от убойных животных (крупный рогатый скот и свиньи) (ГОСТ 11285-73) - для изготовления трипсина;мидии-сырец (ТУ 15-02 279-83) - для изготовления мидийного гидролизата;молоки лососевых рыб (ТУ 9267-037-33620410) - для изготовления дезоксирибонуклеиновой кислоты (ДНК);трипсина импортного (лFerak, Sigma) и отечественного (НПО Вектор) производства - для оценки активности опытно-промышленных партий препарата трипсин;акультуры клеток различного происхождения: первичныеа - куриных эмбрионов (ФКЭ), почек теленка (ПТ)а и перевиваемые линии клеток - почек свиньи (СПЭВ), почек сирийского хомячка (ВНК-1), МсСоу - для оценки диспергирующих свойств опытно-промышленных партий трипсина;апробиотическая кормовая добавка Проваген - дляа изучения влиянияа комплекса этого пробиотика с хитозаном на микробиоценоз толстого кишечника, динамику живой массы и морфо-биохимические показатели гомеостаза телят черно-пестрой породы 1Ц1,5-месячного возраста;апроизводственные штаммы P.multocida трех серовариантов: А - штамм 1231, В - штамм 681 и Д - штамм Т-80 - для оценки флокулирующих свойств хитозана; полупроницаемые мембраны в виде полых волокон из полиамида с пределом задержания по белку 15, 30 и 100 кДа - для очистки и концентрирования биологически активных веществ;
Протеолитическую активность трипсина определяли по методу Kunitz et al. с использованием субстрата казеина по Гаммерстену (1991 г.).
Степень дезацетилирования хитозанаопределяли модифицированныма методом Ван-Слайкаа иа кондуктометрическима титрованием.
Молекулярную массу хитозанаопределялиа с использованием капиллярного вискозиметра Убеллоде с диаметром капилляра 0,71 мм.
Динамическую вязкость растворов хитозана определяли на ротационных вискозиметрах ReotestФ, У Reotest-2Ф и аБрукфилда.
Контроль готовых препаратов проводили в соответствии с ТУ.
а Антиоксидантную активность мидийного препарата определяли амперометрическиа на приборе аЯуза 01.
Статистическую обработку результатов(с числом повторова n? 3)а проводили методами Кербера в модификации Ашмарина, наименьших квадратов, статистических критериев Стьюдента-Фишера (t-критерий) и Кокса-Стюарта с использованием стандартных программ MATHCad-2001.
3. Результаты исследований
3.1. Разработка промышленных технологий изготовления хитозана и его производных для практического применения в различных областях народного хозяйства. аПрименение хитозана в медицине, пищевой промышленности, ветеринарии и некоторых других областях требует строго определенных характеристик препарата. Проведенный нами сравнительный анализ образцов хитозана отечественныха производителей показал, что препарат значительно отличается по качественным характеристикам. Функциональные свойства хитозана (сорбция, биологическая активность, токсичность и т.д.) зависят от молекулярной массы полимера. Так, хитозан с молекулярной массой до 35 кДа используется в качестве иммуностимулятора, радиопротектора, для покрытия микрокапсул и образования пленок. Полимер с молекулярной массой 30-100 кДа включают в состав БАД, применяют в производстве вакцин и сывороток. В бумажной и текстильной промышленности, а также для очистки сточных вод и сорбции тяжелых металлов целесообразно использование хитозана с диапазоном молекулярной массы 80-250 кДа. В пищевой, косметической промышленности, научных исследованиях преимущественно используют хитозан с молекулярной массой свыше 200 кДа. Поэтому исследования по созданию новых, более совершенных, экономичных и экологически безопасных технологий получения хитозана и его модификаций являются актуальными и имеют важное практическое значение.
3.1.1. Разработка промышленной технологии изготовления низкомолекулярного хитозана. аДля получения низкомолекулярного водорастворимого хитозана с регулируемой молекулярной массой, пригодного для применения в ветеринарии, медицине и биотехнологии совместно с ВНИРО и Центром Биоинженерия РАН нами были проведены исследования, направленные на разработку параметров технологического процесса перекисного гидролиза хитозана. В экспериментах использовали хитозан в виде чешуек размером до 6 мм, молекулярной массой (ММ) 350 кДа и степенью дезацетилирования (СДА) 79,3%. Для повышения реакционной способности хитозана его подвергалиа аморфизации, поскольку известно, что макромолекулы хитозана являются полужесткоцепными и во время проведения осаждения, промывки или при изменении концентрации препарата могут образовываться жидкокристаллические растворы, что отрицательно сказывается на реакционной способности и качестве продукта в целом.
Изменением условий проведения гидролиза хитозана (концентрация перекиси водорода, температура процесса и его продолжительность) удалось снизить его молекулярную массу до 23 кДа (Рисунки 2 и 3).аа

Рис.2 Влияние концентрации перекиси водорода на молекулярную массу гидролизата хитозана (t 45оС)
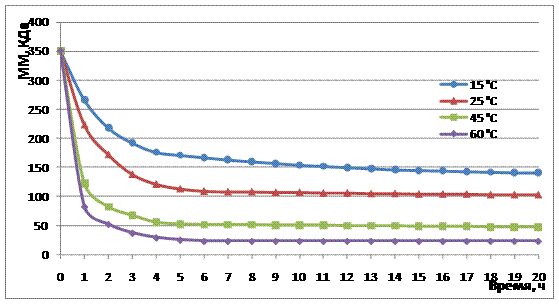
Рис. 3 Влияние температуры на молекулярную массу гидролизата хитозана (0,2 % Н2О2)
аа В качестве оптимальной концентрации перекиси водорода нами была выбрана 0,2%, так кака 0,1% оказалась недостаточной для получения низкомолекулярного хитозана с молекулярной массой 20-50 кДа, а использование 0,3% -ной перекиси водорода при температуре 60оС приводило к появлению в конечном продукте окисленных и модифицированных остатков хитозана.
Процесс гидролиза останавливали добавлением двукратного объема холодной деминерализованной воды (8-10оС) и фильтрацией через бельтинг-ткань, в процессе которой происходила дополнительная очистка низкомолекулярного хитозана от солей и остатков перекиси водорода. Полное удаление перекиси водорода достигалось а2 - 3-кратной промывкой. После лиофильного высушивания полимер имел вид белого аморфного порошка.
В результате проведенных исследований разработана принципиально новая технология получения низкомолекулярного хитозана, включающая стадии гидролиза высокомолекулярного хитозана 0.2%-ной перекисью водорода при температуре 45оС в течение 1,5-2 часов, отделения низкомолекулярного хитозана на рамном фильтре с бельтинг-тканью, растворения при рН 5,5 и лиофильного или распытительного высушивания (рисунок 4).
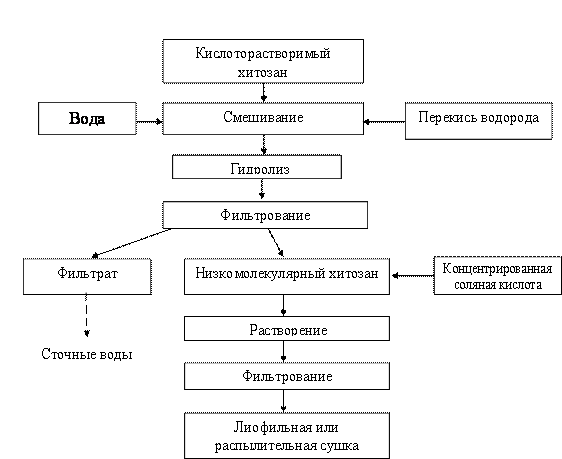
Рис.4. Блок-схема технологического процесса получения низкомолекулярного хитозана методом перекисного гидролиза
Промышленноеа производство низкомолекулярного хитозана освоено на производственном участке отдела получения БАВ ВНИТИБП и в ЗАО Биопрогресс. аГодовой объем производства низкомолекулярного хитозана в зависимости от потребностей составляет до 800 кг.
3.1.2. Разработка промышленной технологии изготовления натриевой соли сукцината хитозана. аНами была разработана технология получения натриевой соли сукцината хитозана, которая заключается в сукцинилировании активированного хитозана янтарным ангидридом, нейтрализации свободных карбоксильных групп янтарной кислоты раствором гидроокиси натрия, фильтрации полученного геля с последующим высушиваниема на распылительной или лиофильной сушке (рисунок 5).
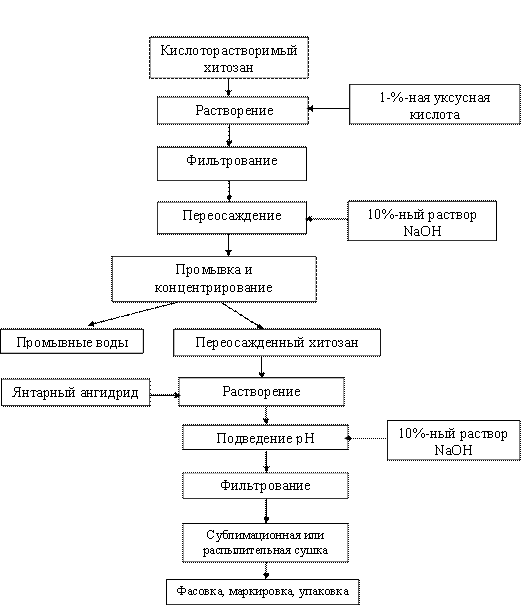
Рис.5. Блок-схема технологического процесса получения натриевой соли сукцината хитозан
а аПри отработкеа параметров технологического процесса основными критериями оценки являлись степень замещения (СЗ)а и выход натриевой соли сукцината хитозана.
На основании результатов органолептических, санитарно-гигиенических, микробиологических и токсикологических исследований натриевой соли сукцината хитозана, изготовленного по разработанной технологии, ва аккредитованном испытательном лабораторном центре при ФГУЗ Центр гигиены и эпидемиологии в городе Москве аиа в аккредитованном испытательном лабораторном центре АНО НИ - Косметология было сделано заключение, что препарат безвреден, ЛД50 при внутрибрюшинном введенииа ?5 г/кг, при накожном ?2,5 г/кг, что позволяет отнести его к IV классу опасности по ГОСТу 12.01.007-76. Препарат не обладает общетоксическим, кожно-раздражающим, сенсибилизирующим действием, физико-химические и микробиологические показатели соответствуют требованиям СанПиН 1.2.681-97 к косметическому сырью.
аа Натриевая соль сукцината хитозана в настоящее время применяется рядом отечественных косметических фирм в качестве биологически активногоа компонента при изготовленииа кремов, гелей, шампуней, бальзамов-ополаскивателей и др. На зубную пасту, содержащую биологически активную добавку хитозан, обладающую противовоспалительным и кариеспрофилактическим действием, а также высокими очищающими и дезодорирующими свойствами, нами был получен Патент РФ №2328267 Зубная паста, приоритет изобретения от 16.01.2007 г.
Для применения в качестве сырья для парфюмерно-косметической продукции были разработаны промышленные технологии изготовления комбинированных препаратов на основе экстрактов бурых водорослей - ламинарии (Ламихит) и фукуса (Фукохит), ассоциированных с хитозаном. Препараты отличаются значительно более высокой биологической активностью благодаря синергизму компонентов, входящих в их состав.
Промышленное производство натриевой соли сукцината хитозана и препаратов на основе экстрактов бурых водорослей налажено ана производственном участке отдела получения БАВ ВНИТИБП и в ЗАО Биопрогресс. В настоящее время годовой объем производства препаратов в зависимости от потребностей составляета 600Ц1000 кг.
3.2. Изучение параметров острой и хронической токсичности хитозана
С целью изучения возможности применения выпускаемого нами хитозана для лечения и профилактики заболеваний животных совместно с А.Р.Таировой был проведен комплекс экспериментов по определению острой и хронической токсичности на мышах. Установлено, что максимально переносимая доза хитозана асоставляет 1600 мг/кг, профилактическая - 70 мг/кг, а терапевтический индекс (соотношение этих доз) - 22,8 , что указывает на достаточный предел безопасного применения препарата в ветеринарной практике.
В соответствии с методикой определения хронической токсичности хитозан вводили в желудок мышей в течение 6 месяцев с 5-дневными интервалами. Показатели содержания гемоглобина, эритроцитов и лейкоцитов в крови, а также гексаналовой пробы, определяющей состояние детоксицирующей функции печени, в опытной группе не отличались от таковых в контрольной .
При гистологическом исследовании внутренних органов от животных, получавших препарат хитозан в течение 6-ти месяцев, существенных изменений, которые можно было бы связать с воздействием препарата на их организм, не обнаружено.
Была исследована зависимость токсических свойств хитозана от его молекулярной массы. В опытах использовались белые мыши в возрасте 2-2,5 месяцев и массой тела 18-22 г. Препараты хитозана вводились однократно в виде 2 % растворов в уксусной кислоте. Контрольным животным также однократно вводили водный раствор уксусной кислоты с рН 5,8. Наблюдение за животными после инъекций испытуемых препаратов проводилось в течение 3 недель. Величину ЛД50 для препаратов хитозана вычисляли по методу Кербера. Как показали результаты исследований, фракции хитозана с молекулярной массой 0-5, 5-10, 10-20 кДа обладают значительно меньшей (в 2-3 раза) токсичностью, чема более высокомолекулярные фракции (с ММ от 20 кДа и более).
3.3.Изучение радиопротекторных свойств хитозана. аИзучение радиопротекторных свойств хитозана проводили совместно с Лысенко Н.П. (МГАВМиБ им. К.И.Скрябина)а на мышах-самцах весом 20-25 г, подвергнутых гамма-облучению на установке Гамма-панорама (источник излучения - 137Сs, мощность излучения - 14 Р/мин, длительность облучения - 58,5 мин). Было сформировано 4 опытных и 2 контрольных группы животных по 7 голов в каждой. Контроль I - облученные животные, контроль II - животные облучению не подвергались. Животным опытных групп вводили внутрибрюшинно хитозан (ММ 5-10 кДа) в дозе 200 мг/кг живой массы: I опытная группа - за 3 дня до облучения, II, III и IV опытные группы - через 3, 9 и 22 дня после облучения, соответственно. Сроки введения хитозана обоснованы основными стадиями лучевой болезни.
Результаты изучения радиопротекторных свойств хитозана представлены на рисунке 6. Полученные результаты свидетельствуют о положительном профилактическом и лечебном эффекте низкомолекулярного хитозана при гамма-облучении мышей в летальных дозах.

Рис.6. Радиопротекторные свойства хитозана
3.4. Практические аспекты применения хитозана и его производных в различных областях народного хозяйства
3.4.1. Применение различных форм хитозана в ветеринарной практике
В хозяйствах Московской, Курской и Тульской областей в период массовых отелов и опоросов проведена серия опытов по изучению эффективности применения хитозана для лечения и профилактики желудочно-кишечных заболеваний молодняка сельскохозяйственных животных.
Совместно с Шинкаревым С.М. испытывался хитозан с различной молекулярной массой (80 кДа, 150 кДа, 300 кДа, 380 кДа, 500 кДа) и растворимостью (кислоторастворимый и водорастворимый), оптимизировались схемы лечения и профилактики (продолжительность, кратность и способ применения), уточнялась доза препарата. Контролем служили группы телят и поросят, которым вводили антибиотики или не назначали лечебный препарат.а Лечебный эффект хитозана оценивали по клиническому состоянию животных, среднесуточному привесу массы тела, по продолжительности течения болезни, проценту вылеченных или павших животных и по биохимическим показателяма крови.
Первые опыты были проведены совместно со специалистами Курского облветуправления в хозяйствах Фатежского района Курской области на телятах с желудочно-кишечными заболеваниями. Использовали 2-3%-ныйа гелевый раствор хитозана с молекулярной массой 300-500 кДа с различными схемами применения. Лечебный эффект наблюдали при выпаивании телятам геля хитозана в дозе 40-60 мл 3-4 раза в день перед кормлением. Курс приема составлял 2-5 дней в зависимости от интенсивности проявления диарейного синдрома. После получения разрешения Департамента ветеринарии МСХиП РФ широкие производственные испытания хитозана были продолжены в хозяйствах Тульской и Московской областей (Таблица 1).а
Таблица 1
Эффективность применения кислоторастворимой формы хитозана различной молекулярной массы при лечении и профилактике желудочно-кишечных заболеваний телят в КСХП Приупское Тульской области
Эффективность |
ММ хитозана, кДа |
Кол-во голов |
Время протекания заболевания, сутки |
Привесы за время наблюдения (8 суток), кг |
Примечание |
ечебная |
380 |
29 |
31 |
4,61,2 |
1 гол. Цдиарея после лечения |
150 |
23 |
31 |
4,51,3 |
1 гол. - диарея после лечения |
|
80 |
19 |
31 |
4,61,1 |
1 гол. Цдиарея незначительная |
|
Профилактическая |
380 |
22 |
- |
5,11,7 |
|
150 |
16 |
- |
6,11,4 |
|
|
80 |
24 |
- |
6,11,6 |
|
|
Контроль |
- |
19 |
62 |
4,81,4 |
ЗаболелоЦ4 гол. Пало -2 гол. |
аа Проведенные исследования показали, что хитозан имеет высокую терапевтическую и профилактическую активность при полном отсутствии токсичности и других побочных действий. При его использовании наблюдалось улучшение клинического состояния животных, исчезали признаки диареи, улучшались биохимические показатели крови, в 80 - 90% случаев наступало полное выздоровление животных.
3.4.2. Изучение влияния хитозана на резистентность сельскохозяйственных животных. аДля изучения влияния гелевого раствора хитозана на резистентность животных и оптимального режима его применения в УОХ Кокино Выгоничского района Брянской области на свиньях крупной белой породы совместно со специалистами Брянской ГСХА был проведен научно-хозяйственный опыт. Были сформированы с учетома возраста, живой массы и продуктивности за предыдущий опорос три группы аналогов - свиноматок крупной белой породы по 3 головы в каждой (А. Б и С группы, соответственно). Свиноматкам С группы дважды (с 6-го и 22-го дня после опороса) утром и вечером по 5 дней выпаивали 2%-ный гелевый раствор хитозана в 1%-ной уксусной кислоте в дозе 3 мл/кг живой массы, свиноматкам А и В групп хитозан не скармливали.а Поросят от свиноматок А, В и С групп обозначили, соответственно, как 1 (контрольная)- хитозан не скармливали, 2 и 3(опытные)- дважды (на 30-й и 45-й день после рождения) утром и вечером по 5 дней вместе с подкормкой скармливали по 3 мл/кг живой массы 2%-ного гелевого раствора хитозана. Всем подопытным животным скармливали основной рацион (и подкормку) согласно рекомендуемым для данной половозрастной группы нормам. Контрольные индивидуальные взвешивания поросят проводили на 1, 30 и 60 сутки после рождения. Перед отъемом (в возрасте 60 суток) у подопытных поросят (по 6 голов из группы) были отобраны пробы крови для анализа.
Была установленаа отчетливая тенденция увеличения выживаемости поросят во второй месяц жизни. При скармливании животным гелевого раствора хитозана за весь опытный период наибольший ростостимулирующий эффект аотмечается при скармливании хитозана только поросятам. (Рисунок 7 и 8). К 2-месячному возрасту количество эритроцитов в кровиа у всех исследованных животных было практически одинаковым,а содержание гемоглобина превышало значения физиологической нормы, причем у животных, получавших препарат хитозана, было выше, чем у контрольных животных. Со
держание лейкоцитов в крови поросят, получавших хитозан, соответствовало верхней границе физиологической нормы, при этом у контрольных животных этот показатель был значительно выше.
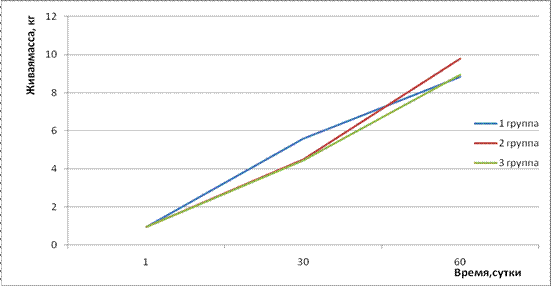
Рис.7 Динамика живой массы поросят при различных формах скармливания гелевого раствора хитозана
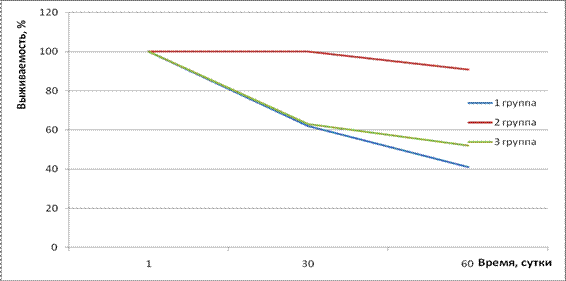
Рис.8 Выживаемость поросят в зависимости от способа скармливания хитозана
3.4.3. Применение хитозана в составе кормовых добавок для сельскохозяйственных животных и птицы. В условиях современного животноводства и птицеводства значительно усилилась технологическая и микробиологическая нагрузка на организм животных и птицы. При этом среди причин отхода молодняка основное место занимают болезни желудочно-кишечного тракта, возбудителями которых являетсяа условно-патогенная микрофлора. Баланс кишечной микрофлоры аможет быть восстановлен с помощью пробиотиков - кормовых добавок,а представляющих собой одну или несколько стабилизированных культур симбиотических микроорганизмов. Помимо пробиотиков, имеется и другая группа препаратов, имеющих разную биологическую природу и механизм действия (кормовые антибиотики, ферменты, пребиотики и др.). Все эти препараты влияют на здоровье и продуктивность животного сходным образом - через регулирование микробной популяции в желудочно-кишечном тракте. К их числу может быть отнесен и хитозан.
Совместно со специалистамиа Брянской ГСХА (Крапивина Е.В.) было изучено влияние выпаивания разных доз пробиотика Проваген, в состав которого входят пробиотические штаммы сапрофитных бактерий B.subtilis ВКМ В-2287 иа B.licheniformis ВКМ В-2414, и комплекса этого пробиотика с хитозаном на микробиоценоз толстого кишечника, динамику живой массы и морфо-биохимические показатели гомеостаза телят.
В МТФ СПК Агрофирма Культура был проведен анаучно-хозяйственный опыт. С учетом живой массы и интенсивности роста методом парных аналогов были сформированы а3 группы ателят черно-пестрой породы 1 - 1,5-месячного возраста: 1 группа - контрольная, 2 и 3 - опытные. Телятам 2 группы ежедневно в течение 7 суток выпаивали пробиотик Проваген (14 г/голову), животным 3 группы - комплекс этого пробиотика (14 г/голову) с хитозаном (0,8 г/голову). Телята содержались в соответствующих ветеринарно-зоогигиеническим требованиям условиях, получали хозяйственный рацион в соответствии с общепринятыми нормами. Через 5 суток после окончания выпаивания препаратов у 3 голов из каждой группы брали содержимое прямой кишки для анализа микробиоты.
Как показали результаты исследований, выпаивание в течение 7 суток Провагена с хитозаном обусловило тенденцию к оптимизации в содержимом толстого кишечника телят уровня эшерихий.
Живая масса у телят 2 и 3 подопытных групп в начале эксперимента существенно не различалась, при этом через 14 суток опыта отмечена тенденция к повышению асреднесуточных приростов живой массы на 10,64% и 21,28%, соответственно, по сравнению с контролем. Комплекс пробиотика с хитозаном в этом отношении оказался более эффективным. (Рисунок 9).
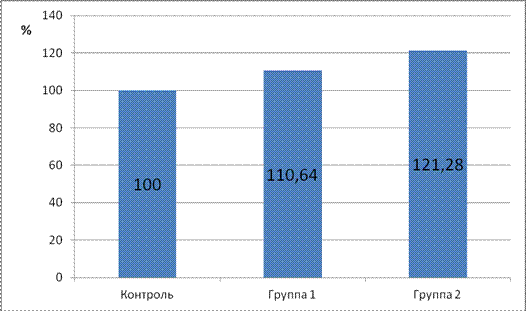
Рис.9 Влияние выпаивания 1-1,5 месячным телятам пробиотика Проваген и комплекса этого пробиотика с хитозаном на среднесуточные приросты живой массы
В результате анализа проб крови животных подопытных групп установлено, что перед началом опыта содержание лейкоцитов, эритроцитов и гемоглобина соответствовало нормативным значениям и по окончании его существенно не изменялось.
Содержание общего белка в сыворотке крови телят всех подопытных групп перед началом опыта соответствовало нижним границам физиологических значений без существенных межгрупповых различий. Выпаивание 1Ц1,5-месячным телятам пробиотика Проваген и комплекса этого пробиотикаа с хитозаном аобусловило оптимизацию гомеостаза, на что указывает увеличение общего белка и снижение билирубина в сыворотке крови. Добавка хитозана к пробиотику обусловила повышение уровня гуморальной защиты организма за счет повышения уровня ?-глобулинов в сыворотке крови. аа
аа Изучение влияния хитозана в составе рациона кормления на продуктивность цыплят-бройлеров проводили в условиях структурного подразделения Околицаа ОАО Птицефабрика им. Н.К.Крупской Республики Беларусь. аа
Таблица 2
Схема опыта по изучению влияния хитозана на продуктивность цыплят-бройлеров кросса Гибро
Группа |
Количество голов |
Условия кормления |
1 (контрольная) |
7000 |
Основной рациона - О.Р. (полнорационный комбикорм для цыплят-бройлеров соответствующего возраста) |
2 (опытная) |
7000 |
О.Р. + хитозан ( 3 мг/гол с 32-х дневного возраста) |
3 (опытная) |
7000 |
О.Р. + хитозан ( 5 мг/гол с 32-х дневного возраста) |
а За весь период опыта сохранностьа птицы в контрольной, 1 и 2 опытных группах составляла 92,1; 92,4 и 92,6 %, количество павшей птицы 7,9; 7,6 и 7,4 %, получено прироста живой массы 883; 1165 и 1153 г, живая масса в конце опыта составила 2210,055,19; 2545,6095,54 и 2626,00 71,57, соответственно. Наблюдаемое положительное влияние хитозана в составе рациона кормления цыплят-бройлерова на их продуктивность возможно связано со способностью хитозана при поступлении с пищей обволакивать стенки слизистой кищечника, адсорбировать и выводить из организма микотоксины, ионы тяжелых металлов, продукты метаболизма бактерий.
Исходя из условий эксперимента, наиболее оптимальной дозой хитозана является ежедневное выпаивание раствора хитозана из расчета 5 мг/голову, начиная с 32-х дневного возраста.
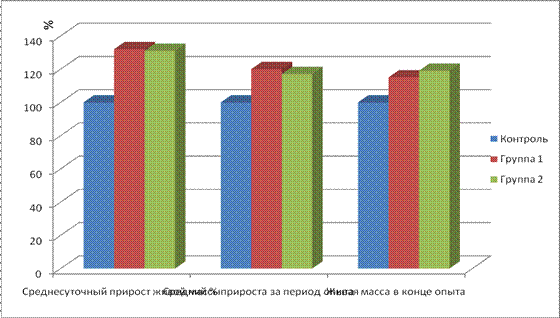
Рис.10 Динамика живой массы и среднесуточных приростов цыплят бройлеров при введении в корм хитозана
аа 3.4.4. Применение хитозана в качестве флокулянта при концентрировании бакмассы P.multocida. Флокулирующие свойства хитозана изучали на производственных штаммах P.multocida трех серовариантов: А - штамм 1231, В - штамм 681 и Д - штамм Т-80 в цехе № 4 ФГУП Щелковский биокомбинат. На первом этапе исследований было установлено, что наилучшие флокулирующие свойства проявляют 1%-ные растворы хитозана, что соответствует 0,02% в пересчете на сухое вещество, а оптимальное значение рН находится в пределах 5,5-6,2. Наиболее полный эффект флокуляции наблюдали в 10 - 12-часовых культурах пастерелл, при этом 4 - 8-часовые культуры в той или иной степени также взаимодействовали с хитозаном.
Изучалась эффективность процессов флокуляции в зависимости от температуры реакционной среды (4, 22 и 370С), молекулярной массы хитозана ( хитозан с ММ 2, 10 и 35 кДа оказался недостаточно эффективным) и степени дезацетилирования (79-97 %). Осаждение клеток пастерелл проходило эффективно при использовании растворов хитозана с ММ в диапазоне 50-500 кДа. После внесения хитозана образование осадка происходило уже через 1-2 минуты. Полностью процесс заканчивался за 24 часа. Увеличение экспозиции до 48-27 часов не давало положительного результата.
Из полученных данных следует, что характер и степень флокуляции клеток P.multocida различных серовариантов зависит от целого ряда факторов ( атемпературы взаимодействия клеток с флокулянтом, ММ хитозана, СДА и др.). Однако при всем многообразии условий эксперимента можно выявить некоторые общие закономерности. Клетки серовариантов P.multocida на различных сроках роста популяций эффективнее связываются хитозаном по мере увеличения его молекулярного веса, при этом температура осаждения заметно снижается. В целом сравнительный анализ выявил относительно ограниченную активность хитозана с ММ 500 кДа. Следует отметить, что наиболее активным для концентрирования клеток P.multocida являются растворы хитозана с ММ 50 кДа (СДА 85%), 100 кДа (СДА 85%) и 250 кДа (СДА 79%). В данных экспериментальных условиях выявлена зависимость степени связывания культур пастерелл от серовариантной принадлежности штаммов. В порядке возрастания эффективности связывания бактерий хитозаном штаммы можно расположить следующим образом: А. В и Д. Последнее, скорее всего, объясняется особенностями морфологии клеток каждого сероварианта.
На основании полученных результатов можно сделать заключение о авысоких сорбционных свойствах хитозана в отношении бактерий вида P.multocida и возможности его использования в технологическом процессе концентрирования бакмассы.
3.4.5. Применение хитозана в технологии получения протеолитического ферментного препарата трипсин. аСогласно оценке российских аналитиков, в настоящее время в нашей стране потребность промышленности в ферментных препаратах удовлетворяется за счет импорта более чем на 90%.
Разработанная нами технология получения трипсина включает стадию измельчения на коллоидной мельнице предварительно дефростированной при +15 - +25оС поджелудочной железы от убойных животных - крупного рогатого скота и свиней, получения экстракта трипсина с одновременным удалением из него балластных веществ в виде белково-липидного комплекса с использованием в качестве осадителя кислоторастворимого хитозана с молекулярной массой 150-250 кДа и нормой ввода 0,4-1,2 литра 1%-ного раствора хитозанаа на 1 кг поджелудочной железы, фильтрацию экстракта трипсина через бельтинг-ткань и ультрафильтрацию раствора через полупроницаемые мембраны в виде полых волокон из полиамида с пределом задержания по белку 15, 30 и 100 кДа, что обеспечивает необходимую степень очистки и концентрирования раствора трипсина перед его лиофильным высушиванием. Технология отличается простотой, полным исключением применения органических растворителей и солей-осадителей ферментов, воспроизводимостью и сравнительно низкими трудозатратами. Основные технологические операции могут быть осуществлены на отечественном оборудовании (рисунок 11).
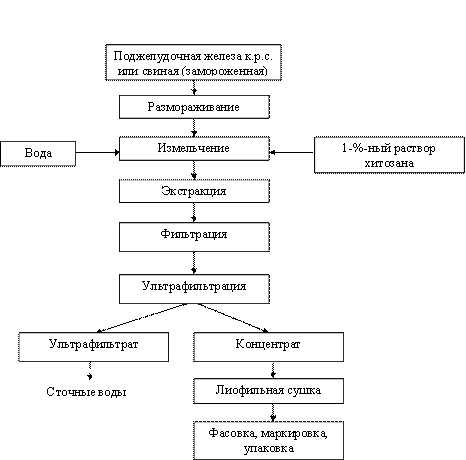
Рис. 11. Блок-схема технологического процесса получения трипсина
аа Применение в качестве осадителя кислоторастворимого хитозана позволило в несколько раз увеличить выход целевого продукта, повысить его активность и сократить время изготовления а(Патент № 2265053 Способ получения трипсина, приоритет изобретения от 24.12.2002 г.). Разработан способ иммобилизации трипсина (Патент № 2437936 Способ иммобилизации трипсина, приоритет изобретения от 17.06.2010 г.).
Испытания эффективности трипсина для диспергирования тканей животных и птиц при получении культур клеток в производственных условиях (ФГУП Ставропольская биофабрика, ФГУП Армавирская биофабрика, ОАО Покровский завод биопрепаратов) показали, что испытуемый препарат не токсичен и обладает активными диспергирующими свойствами. Морфология клеток в культурах была без зернистости и признаков дегенерации.
Опытно-промышленный выпуск ферментного препарата трипсина налажен в условиях опытного производства в отделе получения БАВ ВНИТИБП и в ЗАО Биопрогресс.
3.5.Разработка промышленной технологии изготовления дезоксирибонуклеиновой кислоты (ДНК) и практические аспекты ее применения.
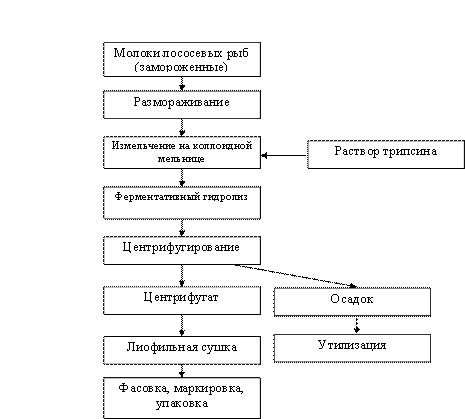
Разработанный нами способ изготовления ДНК отличается высокой производительностью, возможностью масштабирования процесса, позволяющего получать высокий выход и снизить стоимость целевого продукта. В качестве исходного сырья для получения дезоксирибонуклеиновой кислоты используются замороженные молоки лососевых рыб. Схема технологического процесса получения ДНК представлена на рисунке 12.
При отработке параметров технологического процесса основными критериями оценки являлись содержание основного вещества в препарате ДНК и выход готового продукта. Было изучено влияние на эти показатели таких параметров, как соотношение компонентов реакционной смеси, температура и продолжительность процесса. Полученный продукт характеризуется следующими показателями: внешний вид - аморфный порошок; цвет - от белого до светло-коричневого; запах - свойственный данному продукту с рыбным оттенком; массовая доля влаги, %, не более - 8,0; массовая доля основного вещества, %, не менее - 40,0.
 аа
аа
Рис.12. Блок-схема технологического процесса получения ДНК
Лабораторные испытания ДНК, изготовленной по разработанной нами технологии, в аккредитованном испытательном лабораторном центреа ФГУЗ Центр гигиены и эпидемиологии в городе Москве показали, что препарат по санитарно-гигиеническим и микробиологическим показателям соответствует требованиям СанПиНа 1.2.681-97 Гигиенические требования к производству и безопасности парфюмерно-косметической продукции и МУ 05 РЦ/3140. По параметрам острой токсичности сырье косметическое Кислота дезоксирибонуклеиновая из молок лососевых рыб относится к малоопасным веществам (4 класс опасности по ГОСТ 12.1.007-76) при внутрижелудочном пути поступления. В 50% концентрации не оказывает раздражающего действия на кожные покровы при однократном и повторном воздействии, раздражает слизистую оболочку глаз: 2 балла (гиперемия коньюктивы - 1 балл, отек века - 1 балл). В условиях проведенного эксперимента сенсибилизирующее действие не было обнаружено. В настоящее время ДНК в качестве биологически активной добавки введена в состав кремов, гелей и другой косметической продукции, где оказывает геронтологическое действие на метаболические процессы, протекающие в коже.
Промышленное производство ДНК в настоящее время освоено на производственном участке отдела получения БАВ ВНИТИБП и в ЗАО Биопрогресс с годовым объемом производства в зависимости от потребностей а100-150 кг.
аа 3.6. Разработка промышленной технологии получения Мидийного гидролизатаа и изучение эффективности его применения для повышения резистентности молоднякаа сельскохозяйственных животных и птицы. Биологически активные добавки в жизни животного играют важную роль - при крайне малых дозах они способны существенно изменить обмен веществ и повысить общую резистентность организма. В мясе мидий обнаружены соединения, обладающие широким спектром биологической и фармакологической активности. Способность повышать общую резистентность организма связывают с наличием в мидийных препаратах липидных антиоксидантов, меланоидинов и микроэлементов. Широкое применение нашли кислотные и ферментативные гидролизаты мидий. Учеными ВНИРО разработан Мидийный гидролизат кислотный лечебно-профилактический (МИГИ-К-ЛП), промышленное производство которого было налажено во ВНИТИБП-ЗАО Биопрогресс. С цельюаа оптимизации технологического процесса и увеличения объёмов производства нами была разработана экологически чистая технология получения мидийного гидролизата - биологически активной добавки к пище Мидийный соус. При этом былиа решены вопросы локализации и нейтрализации выбросов, стандартизации препарата и снижения энергозатрат (Патент № 2284708 Биологически активная пищевая добавка из мяса мидий и способ ее получения, приоритет изобретенияа 29.12.2004) (рисунок 13).
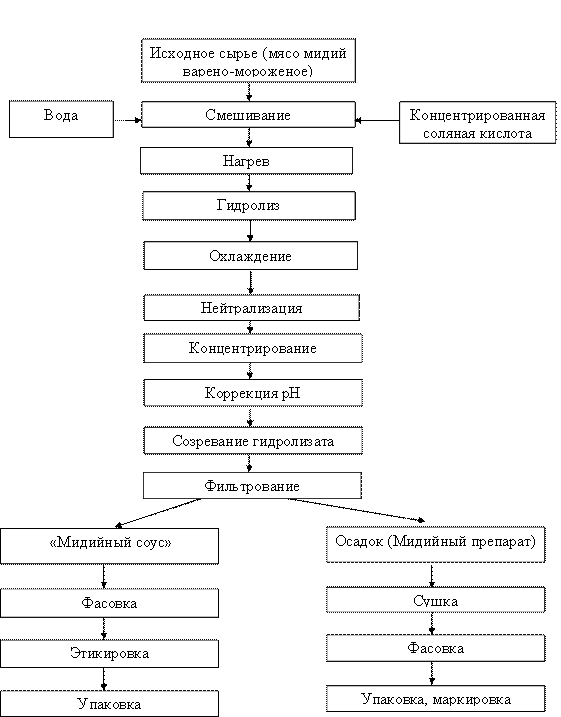
Рис.13. Блок-схема технологического процесса получения мидийного гидролизата
Нами были проведены испытания мидийного препарата, являющегося побочным продуктом при производстве Мидийного соуса, в составе рациона молодняка свиней и птицы.
Изучение влияния Мидийного препарата на рост, развитие и сохранность цыплят проводили на Щелковской птицефабрике на цыплятах породы
кросс П-46 (48710а голов) 6- и 18-суточного возраста и яйценоской породы Родонит (23690 голов) 4-суточного возраста. Мидийный препарат вводили в основной рацион из расчета 1,5 г/кг и 2,0 г/кг живой массы птицы в сутки.
Скармливание Мидийного препарата оказало положительное влияние на рост и развитие молодняка птицы: увеличение среднесуточного прироста живой массы на 4,2-10,9%, снижение затрат корма на 1 кг прироста живой
массы на 3,9-4,4%, уменьшение количества расклевов, приводящих к гибели птицы, что свидетельствует о повышении биологической ценности кормов иа общей резистентности организма.
Изучение эффективности применения Мидийногоа препарата при выращивании молодняка свиней крупной белой породы было проведено на подсвинках 4-месячного возраста со средней живой массой 46,95 кг совместно с Крапивиной Е.В. (Брянская ГСХА) на СТФ СПК Агрофирма Культура Брянской области. Животные контрольнойа группы получали основной рацион, сбалансированный по основным питательным веществам в соответствии с общепринятыми нормами. Животным опытных групп дополнительно к основному рациону ежедневно скармливали Мидийный препарат в дозах 10, 15 и 20 г/кг сухого вещества рациона.
В конце опыта (на 114 день) среднесуточные приросты живой массы в опытных группах по отношению к контрольной были выше на 15,96%-19,45% , затраты корма на 1 кг прироста живой массы ниже на 13,75-16,35%.
В проведенном совместно со специалистами СПК Новое Литвиново (Московская область) научно-хозяйственном опытеа на подсвинках крупной белой породы 4-х месячного возраста (Мидийный препарат скармливали в тех же дозах) через 15 дней после начала опыта было отмечено увеличение прироста живой массы подсвинков на 5,5- 6,3% по сравнению с контролем. Живая масса подсвинков опытных агрупп на 45-й день скармливания была на 7,9%-11,0% больше, чем у животных контрольной группы.
Таким образом, результаты проведенных исследований свидетельствуют об эффективности применения Мидийного препаратаа в качестве биологиче-
ски активной добавки в составе кормаа при выращивании молодняка свиней.аа
Многочисленными исследованиями установлено, что повышение содержания радиоцезия в почвах предопределяет более высокое включение его в ткани животных и снижение под влиянием хронического воздействия радионуклида функциональной активности защитных систем организма.
аа Для изучения влияния Мидийного препарата на резистентность животных, содержащихся в зонах с различной поверхностной активностью почвы по 137Cs и оптимального режима его применения совместно с Крапивиной Е.В. ( Брянская ГСХА) в УОХ Кокино, СТФ СХПК Агрофирма Культура, СТФ СХПК Родина Брянской областиа была проведена серия опытов на свиньях крупной белой породы (свиноматки, поросята 30-суточного, 3-3,5-месячного, 4,5-месячного возраста). Испытывались разные схемы скармливания препарата: свиноматкам с 20-х суток после опороса в течение 5 дней вместе с кормом 0,5 литра на голову разведенного водой (1:3) Мидийного препарата (I схема); поросятам на 30-е сутки после рождения в течение 10 дней возрастающие дозы, начиная с 30 мл/голову разведенного водой (1:3) Мидийного препарата (II схема); поросятам из расчета 10, 15 и 20 г Мидийного препарата на 1 кг сухого вещества рациона в течение всего периода откорма молодняка свиней (III схема).
По I и II схеме скармливания Мидийный препарат оказывал положительный эффект в отношении выживаемости поросят к 60-дневному возрасту, их средней живой массе, содержания гемоглобина, количества лейкоцитов и уровня ?-глобулинов в сыворотке крови. Наиболее эффективным оказалось непосредственное скармливание препарата только самим поросятам. Скармливание препарата по аIII схеме в течение 45 дней вызвало достоверное повышение среднесуточного прироста живой массы до 34,12% по сравнению с контролем, увеличение содержания гемоглобина, нормализацию содержания лейкоцитов.
На основании научно-хозяйственных опытов, проведенных в различных хозяйствах Брянской области, составлены Методические рекомендации поа
использованию Мидийного препарата при выращивании молодняка свиней.
4. ВЫВОДЫ
- Разработана промышленная технология изготовления низкомолекулярного хитозана (ММ 20-50 кДа) с применением метода перекисного гидролиза.
- Разработана промышленная технология изготовления натриевой соли сукцината хитозана, заключающаяся в сукцинилировании активированного хитозана янтарным ангидридом, нейтрализации свободных карбоксильных групп янтарной кислоты раствором гидроокиси натрия, фильтрации и высушивании раствора натриевой соли сукцината хитозана.
- Определены параметры острой и хронической токсичности кислоторастворимого хитозана (ММ 250 кДа, СДА 88%): максимально переносимая доза - 1600 мг/кг, профилактическая доза - 70 мг/кг, терапевтический индекс - 22,8. В хроническом эксперименте на мышах внутрижелудочное введение раствора хитозана в дозе 70 мг/кг веса тела не привело к изменениям гематологических показателей крови и функционального состояния печени.
- Установлено, что хитозан (ММ 5-10 кДа) обладает профилактическим и лечебным эффектом при гамма-облучении мышей в летальных дозах. Процент выживаемости животных был тем выше, чем на более ранних сроках относительно момента облучения вводился хитозан.
- В экспериментальных условиях показана возможность и отработаны условия применения хитозана в качестве энтеросорбента при желудочно-кишечных заболеваниях молодняка сельскохозяйственных животных: в целях профилактики в виде 2%-ного раствора из расчета 2 мл на 1 кг живого веса за 30 минут до кормления 2 раза в день в течение 2 суток, для лечения в виде 3%-ного раствора из расчета 3 мл на 1 кг живого веса за 30 минут до кормления 3 раза в день в течение 3 суток.
- В экспериментальных условиях изучено влияние выпаивания хитозана в комплексе с пробиотиком Проваген на микробиоценоз толстого кишечника, динамику живой массы и морфо-биохимические показатели гомеостаза телят. Установлено, что ежедневное выпаивание в течение 7 суток 1-1,5-месячным телятам комплекса пробиотика Проваген в дозе 14 г/голову и хитозана в дозе 0,8 г/голову в сутки приводит к оптимизации микробиоценоза толстого кишечника за счет повышения уровня эшерихий, повышение среднесуточных приростов живой массы на 9,62%, а также оптимизацию гомеостаза.
- Установлена зависимость характера и степени флокуляции клеток P. multocida различных серовариантов от молекулярной массы и степени дезацетилирования хитозана. Наиболее активными для концентрирования клеток P. multocida являются растворы хитозана с молекулярной массой 50 кДа (СДА 85%), 100 кДа (СДА 85%) и 250 кДа (СДА 79%).
- Разработана экологически безопасная промышленная технология получения протеолитического ферментного препарата трипсина из поджелудочной железы убойных животных (крупный рогатый скот, свиньи) с использованием в качестве осадителя кислоторастворимого хитозана с молекулярной массой 150-250 кДа. Показана возможность применения трипсина для получения первичных и перевиваемых культур клеток.
- Разработана технология аполучения ДНК из молок лососевых рыб с использованием протеолитического фермента трипсина, позволяющая получать препарат с высоким содержанием основного вещества (50-70%), отличающаяся высокой производительностью, возможностью масштабирования процесса, высоким выходом и низкой стоимостью целевого продукта.
- Разработана экологически безопасная атехнология получения мидийного гидролизата - биологически активной добавки к пище Мидийный соус.
- В условиях научно-хозяйственного опыта показана эффективность применения в составе кормовых рационов мидийного препарата, являющегося побочным продуктом при производстве Мидийного соуса, на рост, развитие и уровень естественной резистентности у молодняка сельскохозяйственных животных и птицы.
аа 5. ПРАКТИЧЕСКИЕ ПРЕДЛОЖЕНИЯ
По результатам исследований разработана и утверждена в установленном порядке следующая нормативно-техническая документация: ТУ 9289-008-11734126-05 Хитозан; ТУ 9289-067-00472124-01 (Изменение № 1) Хитозан пищевой; ТУ 9284-027-11743126-08 Сукцинат хитозана;ТУ 9284-026-11734126-08 Ламихит (экстракт ламинарии с хитозаном); ТУ 9284-025-11734126-08 Фукохит (экстракт фукуса с хитозаном); ТУ 9154-030-11734126-10 Кислота дезоксирибонуклеиновая из молок лососевых рыб ; ТУ 9289-029-11734126-09 Биологически активная добавка Кислота дезоксирибонуклеиновая из молок лососевых рыб; ТУ 9283-021-11734126-07 Мидийный соус; Инструкция по применению лекарственного средства Хитозан для лечения и профилактики желудочно-кишечных заболеваний молодняка сельскохозяйственных животных (Регистрационный номер ПВР-2-2.6/01705 от 15 мая 2007 года); Технологический регламент на производство ферментного препарата трипсин; Методические рекомендации по применению трипсина в биотехнологии при производстве препаратов ветеринарного назначения; Методические рекомендации по использованию хитозана в качестве флокулянта при производстве вакцин P.multocida; Методические рекомендации по использованию биологически активной кормовой добавки Мидийный препарат при выращивании молодняка свиней.
На разработанные препараты в государственных регистрационных органах получены: Свидетельство о государственной регистрации лекарственного средства для животных Хитозан (Регистрационный номер ПВР-2-2.6/01705 от 15.05. 2007 г.); Свидетельство о государственной регистрации биологически активной добавки Хитозан пищевой № 77.99.23.3.У.5797.6.09 от 10.06.2009 г.; Санитарно-эпидемиологическое заключение на Изменение № 1 ТУ 9289-067-00472124-03 Хитозан пищевой № 77.99.23.003.Т.001570.06.09 от 10.06.2009 г.; Санитарно-эпидемиоло-гическое заключение на ТУ 9284-027-11734126-08 Сукцинат хитозана № 77.99.40.915.Т.003096.12.08 от 18.12.2008 г.; Санитарно-эпидемиологическое заключение на ТУ 9284-026-11734126-08 Ламихит (экстракт ламинарии с хитозаном) № 77.99.40.915.Т.003098.12.08 от 18.12.2008 г.; Санитарно-эпидемиологическое заключение на ТУ 9284-025-11734126-08 Фукохит (экстракт фукуса с хитозаном) № 77.99.40.915.Т.003099.12.08 от 18.12.2008 г.; Санитарно-эпидемиологическое заключение на сырье косметическое Сукцинат хитозана, Экстракт мидий, Фукохит (экстракт фукуса с хитозаном), Ламихит (экстракт ламинарии с хитозаном) № 77.99.40.915. Д.013950.12.08 от 18.12.2008 г.; Санитарно-эпидемиологическое заключение на ТУ 9154-030-11734126-08 Кислота дезоксирибонуклеиновая из молок лососевых рыб № 77.99.40.915.Т.001476.05.10.12.08 от 26.05.2010 г.; Свидетельство о государственной регистрации биологически активной добавки Кислота дезоксирибонуклеиновая из молок лососевых рыб № 77.99.11.3.У.11192.12.09 от 04.12.2009 г.; Санитарно-эпидемиологическое заключение на ТУ 9289-029-11734126-09 биологически активная добавка Кислота дезоксирибонуклеиновая из молок лососевых рыб № 77.99.11.003.-Т.003227.12.09 от 04.12.2009 г.; Санитарно-эпидемиологическое заключение на ТУ 9283-021-11734126-07 Мидийный соус № 50.99.01.928.Т.-008693.06.07 от 04.06.2007 г.; Санитарно-эпидемиологическое заключение на Мидийный соус № 50.99.01.928.П.009485.07.07 от 17.07.2007 г.
На производственных площадях ВНИТИБП - ЗАО Биопрогресс осуществляется промышленный выпуск: лекарственного средства для животных Хитозан; пищевого сырья Хитозана пищевого, Хитозана низкомолекулярного пищевого, Кислоты дезоксирибонуклеиновой из молок лососевых рыб; косметического сырья Сукцината хитозана, л Ламихита (экстракта ламинарии с хитозаном), Фукохита (экстракта фукуса с хитозаном), Кислоты дезоксирибонуклеиновой из молок лососевых рыб; биологически активной добавки Мидийный соус.
6. СПИСОК ОСНОВНЫХ ПУБЛИКАЦИЙ ПО ТЕМЕ ДИССЕРТАЦИИ
6.1. Список научных публикаций ва рецензируемых журналах,
рекомендованных ВАК Министерства образования и науки РФ
- Самуйленко А.Я. Различные виды хитозана для ветеринарии и животноводства/ А.Я. Самуйленко, С.М. Шинкарев, А.И. Албулов, М.А. Фролова, Е.В. Крапивина, П.А.а Кузнецов // Аграрная Россия, М., 2004, С. 8-12.
- Албулов А.И. Разработка и расширение сферы применения биологически активных препаратов на основе сырья природного происхождения/ А.И. Албулов, М.А. Фролова, А.Я. Самуйленко, В.И. Еремец и др. // Вестник биотехнологии и физико-химической биологии имени Ю.А.Овчинникова. - 2006. - № 2. - С. 33-34.
3. Кржижановская Е.В. Адсорбционные и адъювантные свойства хитозана/ Е.В.Кржижановская, А.И. Албулов, А.Я. Самуйленко, С.М. Шинкарев, Л.С. Люлькова, М.А. Фролова, Н.А. Бондарева, А.В. Гринь, В.Б. Хабаров // Ветеринария и кормление.- 2008.- № 4.- С. 34-35.
4. Кржижановская Е.В. Антимикробный эффект кислоторастворимого хитозана/ Е.В.Кржижановская, А.И. Албулов, Е.А. Рубан, А.И. Албулов, А.Я. Самуйленко, С.М. Шинкарев, М.А. Фролова, В.И. Еремец, Н.А. Бондарева, В.Б. Хабаров, А.В. Гринь // Ветеринария и кормление.- 2008.-№ 5.-С. 14-15.
5. Кржижановская Е.В. Изучение антимикробного действия низкомолекулярных фракций хитозана на микобактерии/ Е.В.Кржижановская, А.В. Гринь, С.М. Шинкарев, М.А. Фролова, А.И. Албулов, Н.А. Бондарева, В.Б. Хабаров, Н.К. Еремец, Е.В. Рахманина, И.А. Бараковский // Ветеринария и кормление.- 2008.-№ 6.-С. 31-33.
6. Кржижановская Е.В. Получение низкомолекулярного хитозана и изучение его антимикробных свойств/ Е.В.Кржижановская, С.М. Шинкарев, М.А. Фролова, А.В. Гринь, А.И. Албулов, Е.А. Рубан, А.В. Гринь // Достижения науки и техники агропромышленного комплекса.-2008.-№ 11.-С. 45-46.
7. Кржижановская Е.В. Изучение антимикробного действия хитозана/ Е.В.Кржижановская, Варламов В.П., А.Я. Самуйленко, А.И. Албулов, С.М. Шинкарев, М.А. Фролова, Н.К. Еремец, Н.А. Бондарева, В.Б. Хабаров, А.В. Гринь // Сельскохозяйственная биология.-2008.-№ 6.-С. 119-121.
8. Антонов С.Ф. Изучение ранозаживляющих свойств хитозана/ С.Ф. Антонов, Е.В.Кржижановская, Ю.И. Филиппов, С.М. Шинкарев, М.А. Фролова // Доклады Российской академии сельскохозяйственных наук.-2008.-№ 6.- С. 52-54.
9. Фролова М.А. Практические аспекты применения хитозана в ветеринарной практике/ М.А. Фролова, А.Я. Самуйленко, А.И. Албулов, В.П. Варламов, С.М. Шинкарев, Н.К. Еремец, А.В. Гринь, В.И. Еремец, А.Г. Мищевцов, И.А. Бараковский // Труды Кубанского государственного аграрного университета.-Серия: ветер. науки.- Краснодар.-2009.-№1 (ч.1.).-С. 300-302.
10. Фролова М.А. Ферментные препараты коллагеназа и трипсин для использования в биотехнологии/ М.А. Фролова, А.И. Албулов, А.Я. Самуйленко // Труды Кубанского государственного аграрного университета.- Серия: ветеринарные науки.-Краснодар.-2009.- №1 (ч.1.).-С.303-304.
11. Фролова М.А. Роль гидролизата из мяса мидий в рационе кормления цыплят/ М.А. Фролова, А.И. Албулов, Н.К. Еремец, Г.Ю. Косовский, Р.В. Рогов // Труды Кубанского государственного аграрного университета. Серия: ветеринарные науки.-Краснодар.-2009.-№1 (ч.2.).-С.346-347.
12. Албулов А.И. Хитансодержащие биологически активные добавки к пище в рационализации питания населения/ А.И. Албулов, М.А. Фролова, О.В. Буханцев, В.М. Быкова, Немцев, С.В. Б.А. Комаров // Рыбпром.-2010.-№ 2.-С. 25-28.
13. Трескунов К.А. Эффективность фитохитодезтерапии и проблемы сертификации фитохитодезов/ К.А. Трескунов, Л.В. Погорельская, А.И. Албулов, М.А. Фролова, Б.А. Комароваа // Традиционная медицин.-Выпуск 5.-2011.-С. 393-394.
14. Фролова М.А. Получение опытно-промышленной партии белкового гидролизата из тушек норок и изучение его токсичности/ М.А. Фролова, А.Я. Самуйленко, А.И. Албулов, В.Н. Денисенко, П.Н. Абрамов, Р.В. Рогов //Матер. Всерос. конф. с междун. участием Экобиотех-2011 и 2-я Всерос. школа-конф. молодых ученых // Известия Самарского научного центра РАН.- Т.13. -№ 5(3). -2011.- С.207-209.
15. Крапивина Е.В. Влияние выпаивания телятам пробиотической кормовой добавки Проваген и хитозана на микробицидную активность нейтрофилов крови/ Е.В. Крапивина, Д.В. Иванов, А.И. Феськов, М.А. Фролова, А.И. Албулов, О.В. Буханцев // Труды Кубанского государственного аграрного университета. Серия: ветеринарные науки.-Краснодар.-2012.-С.
16. Буханцев О.В. Применение хитозана и белковых гидролизатов в комплексе с пробиотиком Муцинол при откорме поросят/ О.В. Буханцев, Р.В. Рогов, М.А. Фролова, А.И. Албулов, А.В. Гринь, П.Н. Абрамов, Р.С. Краснокутский // Свиноводство.-2012.-№ 3.-С.
17. Крапивина Е.В. Хитозан в составе пробиотической кормовой добавки Проваген/ Е.В. Крапивина, Д.В. Иванов, А.И. Феськов, М.А. Фролова, А.И. Албулов, О.В. Буханцев // Ветеринария и кормление.-2012.-№ 1.-С. 30-31.
18. Буханцев О.В. Влияние комплекса хитозан-пробиотик на морфо-биохимические показатели гомеостаза молодняка свиней/ О.В. Буханцев, Р.В. Рогов, М.А. Фролова, А.И. Албулов // Ветеринария и кормление.-2012.-№ 2.-С.32-33.
19. Фролова М.А. аРазработка промышленной технологии изготовления трипсина для биотехнологических целей/ Фролова М.А.а // Вестник Российской академии сельскохозяйственных наук.-2012.-№ 3.-С. 48-49.
6.2. Монография.
20. Албулов А.И. Хитозан в косметике/ А.И. Албулов, А.Я. Самуйленко, М.А. Фролова //Монография Хитин-Хитозан, М., 2002.
6.3. Список патентов
- Способ получения трипсина /А.И. Албулов, А.Я. Самуйленко, А.С. Фоменко, М.А. Фролова, И.Г. Ермишина, С.М. Шинкарев, В.Н. Качалов, А.М. Трунова // Патент РФ на изобретение № 2265053, приоритет от 24.12.2002.-опубл. 27.11.2004.- БИ № 33.
- Патент РФ № 2284708 Биологически активная пищевая добавка из мяса мидий и способ ее получения /А.И. Албулов, М.А. Фролова, С.М. Шинкарев, А.Я. Самуйленко, В.А. Терентьев, Т.А. Телегина //а приоритет от 29.12.2004.-опубл. 10.10.2006.-БИ. № 28.
- Патент РФ № 2328267 Зубная паста / А.И. Албулов, П.Е. Козырев, А.Я. Самуйленко, Е.В. Кондратьев, М.А. Фролова, А.В. Гринь // Патент РФ на изобретение № 2328267, приоритет от 16.01.2007.-опубл. 10.07.2008.-БИ № 19.
- Способ иммобилизации трипсина / В.М. Попова, В.И. Лукина, Е.И. Ярыгина, Л.А. Скороходова, А.И. Гуславский, А.Я. Самуйленко, И.И. Кочиш, И.Н. Матвеева, В.И. Еремец, С.А. Гринь, А.А. Раевский, И.Л. Беро, М.А. Фролова, Н.К. Еремец // Патент РФ на изобретение от 17.06.2010, приоритет от 17.06.2010.-опубл. 27.12.2011.-БИ № 36.
6.4. Список научных публикаций
25.а Фролова М.А Использование хитозана в составе косметических препаратов/ М.А.а Фролова //Мат. IIа Межд. научно-практич. конф.: Биологически активные вещества и новые продукты в косметике М.-1997.- С. 13-14.
26. Албулов А.И. Препараты из мяса мидий как лечебноЦпрофилактические средства при лечении молодняка сельскохозяйственных животных/ А.И. Албулов, А.С. Фоменко, М.А. Фролова, В.Н. Качалов, Е.А. Пилипейко // Мат. Всероссийск. научно-практ. конф., посвященной 70-летию Першина В.А..- Щелково.- ВНИТИБП.- 1998.- С. 36-37.
27. Албулов А.И. Использование хитозана в ветеринарии в составе средств для лечения и профилактики желудочно-кишечных заболеваний у молодняка с/х животных/ А.И. Албулов, А.Я. Самуйленко, М.А. Фролова, А.С. Фоменко, С.М. Шинкарев // Мат. Всероссийск. научно-практ. конф., посвященной 70-летию Першина В.А.- Щелково.- ВНИТИБП.- 1998.- С. 38-39.
28. Сушков И.В. Использование хитозана в растениеводстве/ И.В. Сушков, В.Н. Чикин, А.И. Албулов, М.А. Фролова,а А.С. Фоменко, Е.А.а Е.А.а Пилипейко //Мат. Всеросс. научно-практ. конф., повященной 75-летию со дня рождения Н.Ф.Чуклова.- Щелково.- 1998.- С. 44-45.
29. Бойков П.Я. Проблема удаления запаха из морепродуктов и пути ее решения/ П.Я. Бойков, Б.А. Комаров, А.И. Албулов, М.А. Фролова, Е.А. Пилипейко, Е.А., С.М. Шинкарев, Е.М. Лукьянова//Мат. Всеросс. научно-практ. конф., повященной 75-летию со дня рождения Н.Ф. Чуклова.- Щелково.- 1998.- С. 47-49.
30. Новикова М.В.а Мидийные гидролизаты - новая высокоэффективная лечебно - профилактическая пищевая добавка/ М.В. Новикова, А.С. Фоменко, А.И. Албулов, М.А. Фролова, С.М. Шинкарев,а А.М.а Трунов // Мат. V Российский национ. конгр.: Человек и лекарство.- М.- 1998.- С. 390.
31. Албулов А.И. Хитозан и коллагеназа - биологически активные препараты из морепродуктов и других отраслях народного хозяйства/ А.И. Албулов, А.С. Фоменко, М.А. Фролова, С.М. Шинкарев, Б.А. Комаров, С.В.а Енгашев // Мат. V Российский национ. конгр.: Человек и лекарство.- М.- 1998.- С. 342.
32. Албулов А.И. Мидийные препараты - новые продукты в косметике/ А.И. Албулов, М.А. Фролова, А.С. Фоменко, С.М.а Шинкарев // Мат. III Межд.а научно-практич. конф.: Биологически активные вещества, новые технологии и продукты в косметике.- М.- 1998.- С. 24.
33. Албулов А.И. Новые эффективные лекарственные препараты из сырья природного происхождения/ А.И Албулов, А.С. Фоменко, М.А. Фролова, С.М. Шинкарев, А.М. Трунов // Мат. I Российской научно-практич. конф.: Актуальные проблемы медицинской экологии.- Орел.- 1998.- С. 11-12.
34. Костеша Н.Я.а Производство и контроль медицинских, ветеринарных препаратов, опыт применения и реализации их в странах СНГ/ Н.Я. Костеша, А.К. Дубровский, А.И. Албулов, А.С. Фоменко, М.А. Фролова,а А.В. Кузьминенкова, С.М. Шинкарев // Мат. Межд.а научно-практич. конф.:а Производство и контроль медицинских, ветеринарных препаратов, опыт применения и реализации их в странах СНГ.- Вольгинский.- 1999.- С. 21-23.
35. Албулов А.И. Лечебно-профилактические пищевые добавки из продуктов морского и растительного происхождения/ А.И. Албулов, А.С. Фоменко, М.А. Фролова, В.Н. Качалов, С.М. Шинкарев, А.М. Трунов//Мат. науч. конф.: Место фитотерапии в современной медицине.- Черноголовка.- 1999.- С. 4-7.
36. Новикова М.В. Мидийный гидролизат (МИГИ-К ЛП) как лечебно - профилактический препарат/ М.В. Новикова, А.И. Албулов, А.С. Фоменко, М.А. Фролова, С.М. Шинкарев//Мат. научн. конф.: Место фитотерапии в современной медицине.- Черноголовка.- 1999.- С. 28-31.
37. Албулов А.И. Хитозан - новый препарат для медицины и ветеринарии/ А.И. Албулов, А.Я. Самуйленко, А.С. Фоменко, М.А. Фролова, С.М. Шинкарев, Б.А.Комаров // Мат. VIX Российск. национ. конгр.: Человек и лекарство.-а М.- 1999.- С. 379.
38. Албулов А.И. Применение хитозана в ветеринарии для лечения и профилактики желудочно-кишечных заболеваний молодняка сельскохозяйственных животных/ А.И. Албулов, А.Я. Самуйленко, Н.Э. Нифантьев, А.С. Фоменко, М.А. Фролова, С.М. Шинкарев //Мат. V конф.: Новые перспективы в исследовании хитина и хитозана.- М.- Щелково.- 1999.- С. 115-117.
39. Албулов А.И. Перспективы применения хитозана в косметике/ А.И. Албулов, Л.В. Симонова, М.А. Фролова, Е.А. Пилипейко, А.С. Фоменко//Мат. V конф.: Новые перспективы в исследовании хитина и хитозана М. - Щелково.- 1999.- С. 117-119.
40. Албулов А.И. Разработка новых лечебно-профилактических препаратов из морепродуктов и растительного сырья/ А.И. Албулов, А.Я. Самуйленко, М.А. Фролова, С.М. Шинкарев, Е.А. Пилипейко, А.В. Кузьминенкова // Мат. Всеросс. научно-практич. конф.:а Разработка и освоение производства нового поколения лекарственных средств для животных и их применение в ветеринарной практике.- Ставрополь.- 2000.- С. 70-72.
41. Пилипейко Е.А. Испытания препарата Мидиум в составе рациона кормления цыплят/ Е.А. Пилипейко, А.И. Албулов, М.А. Фролова, М.В. Новикова // Мат. Всеросс. научноЦпрактич. конф., посвящ.а 30-летию ВНИТИБП.- Щелково.- 2000.- С. 339-340.
42. Пилипейко Е.А. К вопросу использования препарата Мидиум при выращивании цыплят/ Е.А. Пилипейко, А.И. Албулов, М.А. Фролова, П.Б. Ершов //Сборник докладов Межд. конф. молодых ученых: Научные основы производства ветеринарных биологических препаратов.- Щелково.- 2001.- С. 174-176.
43. Крапивина Е.В. Состояние защитных механизмов поросят при различных способах использования гелевого раствора хитозана/ Е.В. Крапивина, В.П. Иванов, А.И. Албулов, А.Я. Самуйленко, М.А. Фролова, С.М. Шинкарев //Мат. VI Межд. конф.: Новые достижении в исследовании хитина и хитозана.- М.- 2001.- С. 199-200.
44. Мельник Н.В. Применение хитозана для осаждения клеток пастерелл из бульонных культур/ Н.В. Мельник, Н.Д. Скичко, Е.А. Шубина, А.И. Албулов, А.Я. Самуйленко, С.М. Шинкарев, М.А. Фролова //Мат. VI Межд. конф.: Новые достижении в исследовании хитина и хитозана.- М.- 2001.- С. 217-220.
45. Ершов П.Б. Применение биологически активных добавок из морепродуктов при повышенных физических нагрузках/ П.Б. Ершов, С.М. Шинкарев, В.В. Коржов, М.А. Фролова, А.И. Албулов // Сбор. докл. Межд. конф. молодых ученых: Научные основы технологии производства ветеринарных биопрепаратов.- Щелково.- 2002.- С. 166-168.
46. Албулов А.И. Некоторые аспекты практического применения хитозана и его производных/ А.И. Албулов, М.А. Фролова, С.М. Шинкарев //Ж. Парафармацевтика.- 2002.- № 8.- С. 48.
47. Албулов А.И. Морские водоросли: путь к красоте/ А.И. Албулов, М.А. Фролова //Ж. Сырье и упаковка для парфюмерии, косметики и бытовой химии.- 2002.- № 5 (24).- С. 9.
49. Албулов А.И. Хитозан: строение и свойства/ А.И. Албулов, М.А. Фролова //Ж. Сырье и упаковка для парфюмерии, косметики и бытовой химии.- 2002,.- № 1 (20).- С. 17.
50. Албулов А.И. Мидии для красоты и здоровья нашего организма/ А.И. Албулов, М.А. Фролова //Ж. Сырье и упаковка для парфюмерии, косметики и бытовой химии.-2002.- № 6 (25).-С. 16.
51. Албулов А.И. Новое косметическое сырье из морских водорослей/ А.И. Албулов, М.А. Фролова, О.М. Васильченко //Мат. VII Межд. научно-практ. конф.: Косметические средства и сырье: эффективность и безопасность.- М.- 2002.- С. 37-38.
52. Албулов А.И. Хитозан как средство лечения и профилактики желудочно-кишечных заболеваний молодняка с/х животных/ А.И. Албулов, А.Я. Самуйленко М.А. Фролова, С.М. Шинкарев //Мат. Межд. научно-практич. конф.: Современные вопросы патологии с/х животных.- Минск.- 2003.- С. 33-34.
53. Албулов А.И. Хитозан: вчера, сегодня, завтра/ А.И. Албулов, М.А. Фролова //Мат. VIII Межд. научно-практич. конф.: Косметические средства и сырье: эффективность и безопасность.- М.- 2003.
54. Албулов А.И. Влияние препарата Мидиум в рационе питания молодняка с/х животных и птицы на гематологические показатели/ А.И. Албулов, М.А. Фролова, Е.А. Пилипейко, Е.В. Крапивина, Н.П. Старовойтова //Мат. Межд. научно-практич. конф.: Научные основы производства ветеринарных биологических препаратов.-а Щелково.- 2003.- С. 175-178.
55. Албулов А.И. Эффективность использования препарата Мидиум при выращивании молодняка с/х животных/ А.И. Албулов, М.А. Фролова, Е.А. Пилипейко, Е.В. Крапивина, Н.П. Старовойтова //Мат. Межд. научно-практич. конф.: Научные основы производства ветеринарных биологических препаратов.- Щелково.- 2003.- С. 179-182.
56. Шинкарев С.М. Технологические подходы к стандартизации качества хитозана/ С.М. Шинкарев, А.И. Албулов, А.Я. Самуйленко, М.А. Фролова, А.С. Фоменко, П.А. Кузнецов//Мат. Межд. научно-практич. конф.: Научные основы производства ветеринарных биологических препаратов.- Щелково.- 2003.- С. 183-186.
57. Евтихов П.Н. Сравнительная оценка протеолитической активности ферментных препаратов, получаемых из животного и растительного сырья/ П.Н. Евтихов, С.А. Марушина, Т.А. Потрехалина, А.И. Албулов, М.А. Фролова, А.М.а Трунов //Мат. Межд. научно-практич. конф.: Научные основы производства ветеринарных биологических препаратов.- Щелково.-2003.-С. 195-198.
58. Албулов А.И. Коррекция качества хитозановых препаратов в промышленных условиях/ А.И. Албулов, С.М. Шинкарев, А.Я. Самуйленко, М.А. Фролова, А.С. Фоменко, С.И.а Лебедько //Мат. VII Межд. конф.: Современные перспективы в исследовании хитина и хитозана, С-Пб - Репино.-2003.-С. 9-11.
59. Албулов А.И. Перспективы применения низкомолекулярных хитозанов в производстве БАД/ А.И. Албулов, А.Я. Самуйленко, М.А. Фролова //Мат. V Межд. научной конф.: Фитотерапия, биологически активные вещества естественного происхождения.-Черноголовка.-2004.-С. 312-319.
60.а Фролова М.А. Некоторые направления применения различных форм хитозана в ветеринарной практике/ М.А. Фролова, А.Я. Самуйленко, С.М. Шинкарев, П.А. Кузнецов, Ю.Д. Фролов, А.И. Албулов //Мат. Межд. конф.: Ветеринарная медицина 2005: современное состояние и проблемы обеспечения благополучия животноводства.- Ялта.- 2005.-С. 45-49.
61. Албулов А.И. Получение низкомолекулярного хитозана методом ферментного гидролиза/ А.И. Албулов, С.М. Шинкарев, М.А. Фролова, П.А. Кузнецов, А.В. Гринь, В.П. Варламов, А.В. Ильина, С.В. Немцев //Мат. Межд. научно-практич. конф. Научные основы производства ветеринарных биологических препаратов, посв. 35-летию ВНИТИБП.-Щелково.- 2005.-С. 430-435.
62. Фролова М.А. ДНК из молок лососевых рыб - получение и свойства/ М.А. Фролова, А.И. Албулов, С.М. Шинкарев, А.Я. Самуйленко, О.М. Васильченко, Д.А. Данишевский //Мат. Межд. научно-практич. конф.:а Научные основы производства ветеринарных биологических препаратов, посв. 35-летию ВНИТИБП.- М.-2005.-С. 527-530.
63. Албулов А.И. Влияние скармливания хитозана на резистентность телят и поросят в условиях повышеннойа плотности загрязнения почв радиоцензием/ А.И. Албулов, Е.В. Крапивина, М.А. Фролова,а А.Я. Самуйленко, В.И. Еремец, С.М. Шинкарев, П.А. Кузнецов, А.В. Гринь //Мат. Межд. научно-практич. конф. Актуальные проблемы ветеринарной медицины в условиях современного животноводства.- Минск.- 2005.-С. 62-66.
64. Албулов А.И. Некоторые направления применения различных форм хитозана в ветеринарной практике/ А.И. Албулов, М.А. Фролова, А.Я. Самуйленко, С.М. Шинкарев, П.А. Кузнецов, Ю.Д. Фролов //Межотраслевой научный сборник Ветеринарная медицина.- Харьков.- 2005.- № 85.- Т. 2.- С. 45-49.
65. Фролова М.А. Практические аспекты применения хитозана и его производных в различных областях народного хозяйства/ М.А. Фролова, А.И. Албулов,а В.И. Еремец, С.М. Шинкарев, А.В. Гринь //Мат. VIII Межд. конф. Современные перспективы в исследовании хитина и хитозана.-Казань.- 2006.- С. 68-70.
66. Албулов А.И. Разработка и расширение сферы применения биологически активных препаратов на основе сырья природного происхождения/ А.И. Албулов, М.А. Фролова, А.Я. Самуйленко, В.И. Еремец, Е.В. Шмидт //Мат. IV съезда Общества биотехнологов России им. Ю.А. Овчинникова.- Пущино.-2006.-С. 8-10.
67. Албулов А.И. Хитозансодержащие лечебно-профилактические препараты: настоящее и будущее/ А.И. Албулов, А.Я. Самуйленко, М.А. Фролова, Б.А. Комаров, С.М. Шинкарев, П.А. Кузнецов, Е.В. Шмидт //Мат. VI Межд. научной конференции Фитотерапия, биологически активные вещества естественного происхождения в современной медицине.-Черноголовка.-2006.-С.22-24.
68. Албулов А.И. Опыт применения препаратов хитозана в сельском хозяйстве/ А.И. Албулов, М.А. Фролова, В.П. Варламов, Кузнецов П.А., С.М. Шинкарев, Е.В. Шмидт, Е.И. Лебедько, А.В. Гринь //Мат. Межд. научно-практ. конф., посвященной 80-летию со дня рождения И.А.Харькова Научные основы производства ветеринарных биологических препаратов.- Щелково.-2006.-С. 257-261.
69. Албулов А.И. Сорбционные свойства хитозана и их применение при выращивании молодняка сельскохозяйственных животных и птицы/ А.И. Албулов, С.М. Шинкарев, М.А. Фролова, Е.В. Кржижановская, А.К. Чуклов, А.В. Гринь, Е.В. Шмидт //Сборник научных трудов Основные проблемы ветеринарной медицины и стратегия борьбы с заболеваниями сельскохозяйственных животных в современных условиях.-Махачкала.-2007.-С. 251-254.
70. Албулов А.И. Применение ферментов в технологиях переработки мясных и рыбных производств/ А.И. Албулов, М.А. Фролова, С.А.,а Марушина, Ф.М. Снегур, И.А. Ельцова //Сборник научных трудов Луганского национального аграрного университета.- Луганск.-2008.-№ 87.-С.3-7.
71. Кузнецов П.А. Получение фракций хитозана и изучение их биологических свойств/ П.А. Кузнецов, А.И. Албулов, А.Я. Самуйленко, М.А. Фролова, С.М. Шинкарев, Ю.Д. Фролов // Мат. научно-практич. конф. Пищевая и морская биотехнология: проблемы и перспективы.- Светлогорск.- 2008.-С. 81-82.
72. Фролова М.А. ДНК из молок лососевых рыб - эффективная биологически активная добавка/ М.А. Фролова, А.Я. Самуйленко, А.И. Албулов, В.И. Еремец, О.М. Васильченко // Мат. научно-практич. конф. Пищевая и морская биотехнология: проблемы и перспективы.-Светлогорск.-2008.-С. 140.
73. Албулов А.И. Результаты и проблемы внедрения инновационных технологий на основе хитинсодержащего сырья/ А.И. Албулов, А.Я. Самуйленко, М.А. Фролова, С.М. Шинкарев, В.И. Еремец, А.В. Гринь //Мат. IX Межд. конф. Современные перспективы в исследовании хитина и хитозана.-Ставрополь.- 2008.-С. 7-9.
74. Албулов А.И. Использование хитозана в составе препаратов для лечения и профилактики болезней собак/ А.И. Албулов, М.А. Фролова, С.А.,а Е.В. Шмидт, Л.А. Гасанова, В.Н. Портянко, Е.И. Лебедько //Мат. XVI Моск. Межд. конгресса по болезням мелких домашних животных.-2008.- М.-С. 157-158.
75. Красочко П.А. Влияние низкомолекулярного хитозана на продуктивность и качество продукции от цыплят-бройлеров/ П.А. Красочко, М.А. Фролова, А.И. Албулов, Н.К. Еремец, А.В. Гринь, И.Л. Беро, В.И. Еремец, А.П. Дуктов //Мат. Межд. научно-практ. конф., посвящ. 40-летию ВНИТИБП Научные основы производства ветеринарных биологических препаратов.-Щелково.- 2009.-С. 462-469.
76. Гулик Е.С. Влияние хитозана и хитабиса на состояние надэпителиального слизистого слоя тонкого кишечника/ Е.С. Гулик, Г.А. Костеша, А.И. Албулов, М.А. Фролова //Мат. Межд. научно-практ. конф., посвящ. 40-летию ВНИТИБП Научные основы производства ветеринарных биологических препаратов.-Щелково.-2009.-С. 481-484.
77. Фролова М.А. Гидролизаты белков из сырья животного и растительного происхождения/ М.А. Фролова, А.И. Албулов, А.Я. Самуйленко, Р.В. Рогов, И.Г. Ермишина, И.Л. Беро //Мат. Межд. научно-практ. конф., посвящ. 40-летию ВНИТИБП: Научные основы производства ветеринарных биологических препаратов.-Щелково.-2009.- С. 517-522.
78. Албулов А.И. Современное состояние и перспективы производства хитозан-содержащей продукции в России/ А.И. Албулов, А.Я. Самуйленко, М.А. Фролова, А.В. Гринь, О.В. Буханцев, В.П. Варламов //Мат. X Межд. конф.: Современные перспективы в исследовании хитина и хитозана.-Нижний Новгород.-2010.-С.7-10.
79. Албулов А.И. Влияние способа высушивания на качество продукта при производстве хитозана и хитозансодержащей продукции/ А.И. Албулов, М.А. Фролова, Б.А. Комаров, С.М. Шинкарев, О.В. Буханцев, В.И. Еремец //Мат. 10-й Межд. конференции Современные перспективы в исследовании хитина и хитозана.-Нижний Новгород.-2010.-С. 74-77.
80. Фролова М.А.а Ферментативные гидролизаты из различных видов сырья животного происхождения/ М.А. Фролова, А.И. Албулов, Р.В. Рогов, А.К. Лихотин //Ж. Труды БГУ.-2009.-Т. 4.-ч. 2.-С. 298-300.
81. Фролова М.А. Гидролизаты белков из сырья животного и растительного происхождения/ М.А. Фролова, А.И. Албулов, А.Я. Самуйленко, Р.В. Рогов, И.Г. Ермишина // Сбор. мат. XI Межд. конф. молодых ученых Пищевые технологии и биотехнологии.-Казань.-2010.-Ч. 2.-С.
82. Албулов А.И. Отечественные хитозансодержащие биологически активные добавки/ А.И. Албулов, В.П. Варламов, М.А. Фролова, Б.А. Комаров, О.В. Буханцева //Мат. I Межд. научно-практич.а конф.: Инновационные технологии управления здоровьем и долголетием человека.-2010.-Санкт-Петербург.-С. 10-14.
83. Фролова М.А. Эффективность применения препаратов хитозана при заболеваниях кожи и химических и термических ожогах/ М.А. Фролова, Е.И. Лебедько, С.М. Шинкарев, А.И. Албулов, О.В. Буханцев, Ю.Д. Фролов //Мат. межд. научно-практич. конф.а Актуальные проблемы ветеринарии и животноводства.- 2010.-Самара.- С. 334-337.
84. Комаров Б.А.а Лиофилизация экстрактов лекарственных растений в присутствии хитозана полифракционного состава/ Б.А. Комаров, А.И. Албулов, М.А. Фролова, А.В. Гринь //Каталог докладов IV Межд. конф.: Экстракция органических соединений.-Воронеж.-2010.-С. 95.
85. Фролова М.А. Влияние природного полимера хитозана в составе пробиотических препаратов на состояние здоровья и продуктивность сельскохозяйственных животных и птицы/ М.А. Фролова, А.И. Албулов, А.Я. Самуйленко, А.В. Гринь, Р.В. Рогов //Мат. межд. научно-практич. конф., посвященной 40-летию ГНУ ВНИВИПФиТ:Актуальные проблемы болезней обмена веществ у сельскохозяйственных животных в современных условиях.-Воронеж.-2010.-С.
86. Фролова М.А. Биологические свойства различных форм и модификаций хитозана при использовании их в ветеринарии, животноводстве и агробиологии/ М.А. Фролова, А.И. Албулов, А.Я. Самуйленко, С.М. Шинкарев, О.В. Буханцев, В.П. Варламов, Е.В. Крапивина, Ю.Д. Фролов //Мат. V Межд. конф. Акт. проблемы биологии в животноводстве.-Боровск.-2010.-С. 124-125.
87. Фролова М.А. Разработка технологии изготовления гидролизатов из сырья различного происхождения для использования в животноводстве/ М.А. Фролова, А.И. Албулов, А.Я. Самуйленко, Р.В. Рогов, М.Ю. Тюрмина //Матер. V Межд. конф. Актуальные проблемы биологии в животноводстве.-Боровск.-2010.-С. 109-110.
88. Фролова М.А. Разработка промышленной технологии изготовления фармацевтических препаратов протеолитического действия для использования в различных областях народного хозяйства/ М.А. Фролова, А.И. Албулов, А.Я. Самуйленко, В.П. Варламов, Р.В. Рогов, О.В. Буханцев //Сборник научных трудов Перспективные биокатализаторы для перерабатывающих отраслей АПК.-М.-2010.-С. 123-128.
89. Фролова М.А. Лечебная эффективность хитозановых препаратов/ М.А. Фролова, А.И. Албулов, А.Я. Самуйленко, С.Д. Антонов, С.М. Шинкарев, А.В. Гринь, О.В. Буханцев, Ю.Д. Фролов //Ж. Ветеринарна медицина выпуск 95, Харьков,а 2011, С. 232-233.
90. Фролова М.А. Изучение влияния хитозана в составе рациона кормления на продуктивность цыплят - бройлеров/ М.А. Фролова, А.И. Албулов, А.Я. Самуйленко, О.В. Буханцев, П.А. Красочко //Ж. Ветеринарна медицина выпуск 95.-Харьков.-2011.-С. 414-415.
91. Албулов А.И. Перспективные белковые добавки для обогащения кормового рациона пчел/ А.И. Албулов, М.А. Фролова, Р.В. Рогов, Н.Г. Билаш, С.С. Сокольский //Мат. Межд. научно-практич. конф.:а Пути развития пчеловодства в России через успешный опыт регионов России, стран СНГ и Дальнего Зарубежья.-Ярославль.-2011.-С.76.
92. Албулов А.И. Перспективы получения биологически активных добавок к пище на основе морепродуктов/ А.И. Албулов, М.А. Фролова, А.Я. Самуйленко, В.П. Варламов, В.М. Быкова, О.В. Буханцев // Мат. IVа Межд. конф.: Морские прибрежные экосистемы. Водоросли, беспозвоночные и продукты их переработки.-Южно-Сахалинск.-2011.-С.192-193.
93. Рогов Р.В. Получение продуктов гидролиза белка из сырья растительного происхождения/ Р.В. Рогов, М.А. Фролова, А.И. Албулов //Мат. II Межд. научной конф.: Молодежная наука - пищевой промышленности. Ставрополь.-2011.-С. 151-154.
94. Фролова М.А. аЭкологически безопасные хитозансодержащиеа средства защиты растений для агропромышленного комплекса/ М.А. Фролова, А.И. Албулов, В.П. Варламов, А.Я. Самуйленко, О.В. Буханцев, А.В. Гринь //Мат. Межд. научно-практ. конф. посвященнойа 10-летию факультета пищевых биотехнологий.-Уфа.- 2011.С.
95. Application experience of chitosan in veterinary practice / M.A. Frolova, A.I. Albulov, A.J. Samujlenko, S.M. Shinkarev, O.V. Buhantsev // Adv. Chitin Sci.: the 10th International Conference of the European Chitin Society. - St.-Petetersburg, 2011. - Vol. 11. - P. 8-9.
96. Фролова М.А. Косметическое сырье и морепродукты / М.А. Фролова, А.И. Албулов, О.М. Васильченко, В.И. Еремец, О.В. Буханцев, Р.В. Рогов //Мат. Межд. научно-практ. конф. Пищевая и морская биотехнология для здорового питания и решения медико-социальных проблем.-Светлогорск.-2011.-С. 121-122.
97. Албулов А.И. Хитозан содержащие биологически активные добавки - источники активных компонентов пищи/ А.И. Албулов, М.А. Фролова, В.П. Варламов, А.В. Гринь, О.В. Буханцев, В.М. Быкова //Мат. Межд. научно-практ. конф. Пищевая и морская биотехнология для здорового питания и решения медико-социальных проблем.-Светлогорск.-2011.-С. 6-7.
98. Фролова М.А. ДНК из молок лососевых рыб для применения в качестве БАД в косметической продукции/ М.А. Фролова, А.И. Албулов, О.М. Васильченко, Р.В. Рогов, Ю.Д. Фролов //Мат. Межд. научно-практ. конф. Пищевая и морская биотехнология для здорового питания и решения медико-социальных проблем.-Светлогорск.-2011.-С. 119-120.
99. Фролова М.А.а Изучение эффективности примененияа мидийного гидролизата как кормовой добавки для повышения неспецифической резистентности организма у молодняка свиней М.А. Фролова, А.И. Албулов, А.Я. Самуйленко, Е.В. Крапивина, Р.В. Рогов //Мат. научно-практ. конф., посвященной 90-летию ФГУП Армавирская биофабрика.-Армавир.-2011.-С. 87-91.
100. Фролова М.А.а Перспективы применения хитозана и его производных в составе ветфармпрепаратов/ М.А. Фролова, А.И. Албулов, А.Я. Самуйленко, В.П. Варламов, А.В. Гринь, О.В. Буханцев //Мат. Межд. научно-практ. конф. Фармацевтические и медицинские биотехнологии.-2012.- М.-С. 295-296.
101. Фролова М.А.а Использование метода ультрафильтрации при получении ферментного препарата трипсина для биотехнологических целей/ М.А. Фролова, Р.В. Рогов, А.И. Албулов, Д.С. Немцев, А.В. Гринь //Мат. VI Межд. научно-практич. симпозиума: Перспективные ферментные препараты и биотехнологические процессы в технологии продуктов питания и кормов.-М.-2012.-С. 47-50.
ОСНОВНЫЕ СОКРАЩЕНИЯ
НД - нормативная документация
ТУ - технические условия
ТИ - технологическая инструкция
ОР - основной рацион
ФР - физиологический раствор
ЖКТ - желудочно-кишечный тракт
АА - антиоксидантная активность
БАВ - биологически активное вещество
БАД - биологически активная добавка
кДа - килодальтон
ММ - молекулярная масса
ММР - молекулярно-массовое распределение
СДА - степень дезацетилирования
СЗ - степень замещения
ДНК - дезоксирибонуклеиновая кислота
РНК - рибонуклеиновая кислота
КРС - крупный рогатый скот
ВНКИ-21а - перевиваемая линия клеток почки сирийского хомячка
ПТ - почка теленка
СПЭВ - перевиваемая линия почек свиней
ФКЭа - фибробласты куриных эмбрионов
ИП - индекс пролиферации
 Все авторефераты докторских диссертаций
Все авторефераты докторских диссертаций
