Книга вторая Дж. Эдвард Морган-мл. Мэгид С. Михаил Перевод с английского
| Вид материала | Книга |
- Книга первая Дж. Эдвард Морган-мл. Мэгид С. Михаил Перевод с английского, 10010.77kb.
- А. Конан-Дойль новоеоткровени е перевод с английского Йога Рàманантáты, 2314.23kb.
- Copyright Сергей Александровский, перевод с английского Email: navegante[a]rambler, 619.61kb.
- "книга непрестанности осириса " 177, 7373.41kb.
- Н. М. Макарова Перевод с английского и редакция, 4147.65kb.
- Трудового Красного Знамени гупп детская книга, 2911.61kb.
- Трудового Красного Знамени гупп детская книга, 2911.77kb.
- Уайнхолд Б., Уайнхолд Дж. У 67 Освобождение от созависимости / Перевод с английского, 11462.2kb.
- Малиновской Софьи Борисовны Специальность: журналистика Специализация: художественный, 969.08kb.
- Духовные истины в психических явлениях перевод с английского 3-е издание Москва «Философская, 1557.75kb.
Наиболее тяжелое осложнение однолегочной ИВЛ — гипоксемия. Чтобы снизить риск развития гипоксемии, необходимо минимизировать длительность однолегочной вентиляции и поддерживать FiO2 на уровне 100 %. Если пиковое давление в дыхательных путях превышает 30 см вод. ст., нужно снизить дыхательный объем до 8-10 мл/кг и увеличить частоту дыхания, чтобы минутный объем дыхания остался неизменным. Для мониторинга используют пульсоксиметрию и анализ ГАК в динамике. Показатели ETCO2 могут недостоверно отражать PaCO2 (гл. 6).
При возникновении гипоксемии рекомендованы следующие мероприятия:
Первая ступень
1. Периодическое раздувание спавшегося легкого кислородом.
2. Ранняя перевязка илрт пережатие ипсилате-ралыюй легочной артерии (при пульмонэктомии).
3. ППДДП, 5-10 см вод. ст., в бронхиальном канале (ведущем к коллабированному легкому); эта мера особенно эффективна, когда частично расправленное оперируемое легкое препятствует хирургическрш манипуляциям.
Вторая ступень
1. ПДКВ, 5-10 см вод. ст., в трахеальном канале (ведущем к вентилируемому легкому).
2. Постоянная инсуффляция крюлорода в кол-лабргрованное легкое.
3. Изменение дыхательного объема и частоты дыхания.
Устойчивая гипоксемия — показание к немедленному расправлению коллабированного легкого. Повторные фибробрОНХОСКОПИР! ПОЗВОЛЯЮТ ВЫЯВР1ТЬ
смещение эндотрахеальной трубки (или бронхо-
блокатора) по отношению к килю трахеи. Необходимо регулярно отсасывать отделяемое из обоих просветов трубки во избежание обструкции секретом или твердыми частицами. Если в дыхательных путях есть кровь, то инсталляция 3-5 мл раствора бикарбоната натрия в трубку облегчает удаление сгустков. Нужно исключить пневмоторакс вентилируемого легкого, который может возникать после обширного вскрытия средостения или при высоком пиковом" давлении в дыхательных путях.
^ Методы, альтернативные однолегочной ИВЛ
На короткий промежуток времени вентиляцию можно прекратить, обеспечивая оксигенацию ин-суффляцией чистого кислорода; при этом поступление кислорода должно превышать потребление. Данная методика носит название апнейстическая оксигенация. Апнейстическая оксигенация позволяет длительно поддерживать удовлетворительную оксигенацию, однако прогрессирующий респираторный ацидоз в большинстве случаев ограничивает время ее применения 10-15-ю минутами. PaCO2 возрастает на 6 мм рт. ст. в первую минуту, затем на 3-4 мм рт. ст. в каждую последующую минуту.
Высокочастотная ИВЛ с положительным давлением (синоним — высокочастотная объемная ИВЛ) и струйная высокочастотная ИВЛ используются в торакальной хирургии как альтернатива однолегочной ИВЛ (гл. 50). При высокочастотной ИВЛ применяют стандартную эндотрахе-альную трубку. Низкий дыхательный объем (< 2 мл/кг) обеспечивает полноценную вентиляцию и одновременно уменьшает легочные экскурсии, что облегчает хирургические манипуляции. К сожалению, в ряде случаев колебательные движения средостения затрудняют оперативное вмешательство.
^ 3. ПОСЛЕОПЕРАЦИОННЫЙ ПЕРИОД Общие принципы
Для снижения риска возникновения легочной инфекции и баротравмы (особенно опасна несостоятельность бронхиального шва) показана ранняя экстубация. При значительном уменьшении функционального легочного резерва эндотрахеальную трубку оставляют до тех пор, пока состояние пациента не будет соответствовать стандартным критериям экстубации (гл. 50); при использовании двух-просветной эндобронхиальной трубки ее меняют в конце операции на обычную эндотрахеальную. Если ларингоскопия и интубация при индукции
анестезии вызывали технические трудности, то для смены трубок применяют катетер-проводник ("трубкообменник").
После операции пациентов переводят в палату пробуждения, а затем — в отделение интенсивной терапии, где они находятся по меньшей мере до утра. В послеоперационном периоде часто возникают гипоксемия и дыхательный ацидоз, что обусловлено хирургической травмой легкого и поверхностным дыханием по причине боли от разреза. Накопление жидкости в нижерасположенном легком под действием силы тяжести также приводит к гипоксемии. При быстром раздувании дыхательной смесью высока вероятность отека коллабированного легкого.
Кровотечение осложняет 3 % торакотомий; летальность при этом достигает 20 %. ^ Симптомы кровотечения: увеличение объема отделяемого по торакалъному дренажу (> 200 мл/ч), артериальная гипотония, тахикардия и снижение гематокрита в динамике. Очень часто возникают над-желудочковые тахиаритмии, которые требуют интенсивного лечения (гл. 19 и 48). Острая недостаточность ПЖ проявляется низким сердечным выбросом, высоким ЦВД> олигурией и нормальным Д ЗЛА (гл. 21).
Стандарты ведения в послеоперационном периоде включают полусидячее положение пациента (головной конец кровати приподнят > 30°), окси-генотерапию (ингаляция смеси с FiO2 40-50 %), мониторинг ЭКГ и гемодинамики, рентгенографию грудной клетки, интенсивное лечение боли.
^ Послеоперационная анальгезия
При значительном снижении функционального легочного резерва трудно добиться оптимального соотношения между комфортом пациента и приемлемой степенью депрессии дыхания исключительно с помощью парентерального введения наркотических анальгетиков. Существуют другие методики, которые обеспечивают полноценную анальгезию pi позволяют совсем отказаться от парентерального введения наркотических анальгетиков. Если, тем не менее, принято решение использовать наркотические анальгетики парентерально, то целесообразно применять малые дозы в/в, а не высокие в/м и вводить их с помощью приспособления, управляемого больным (гл. 18).
Инъекция местных анестетиков длительного действия, например 0,5 % бупивакаина (4-5 мл), в межреберные промежутки на два уровня выше и ниже линии торакотомий (т. е. анестетик вводят в четыре межреберных промежутка), обеспечивает адекватную анальгезию. Межреберную блокаду
можно выполнить под контролем зрения во время операции или же в послеоперационном периоде по стандартной методике (гл.17). Межреберная блокада улучшает показатели ГАК и параметры функции внешнего дыхания, а также сокращает продолжительность лечения. Альтернативный метод — криоанальгезия, когда во время операции межреберные нервы подвергают действию низких температур (крионевролиз), что вызывает длительную анестезию. К сожалению, анальгетичес-кий эффект развивается медленно и даже через 24-48 ч после процедуры не всегда достигает максимума. Регенерация нерва после крионевролиза занимает приблизительно 1 мес.
Введение опиоидов в эпидуральное пространство также позволяет добиться полноценной анальгезии. Эффективность морфина одинакова при введении как через торакальный, так и через люмбальный эпидуральный катетер. Чаще используют люмбальный доступ, потому что в этом случае риск травмы спинного мозга или пункции твердой мозговой оболочки значительно ниже. Инъекция 5-7 мл морфина, растворенного в 10-15 мл физиологического раствора, на 6-10 ч обеспечивает анальгезию без вегетативной, сенсорной и моторной блокады. Липофильные опиоиды (например фентанил), наоборот, более эффективны при инъекции в эпидуральное пространство через торакальный, а не через люмбальный катетер (гл. 18). Некоторые клиницисты предпочитают эпидуральное введение фентанила, поскольку он меньше угнетает дыхание; тем не менее тщательный мониторинг необходим при эпидуральном введении любого наркотического анальгетика.
Есть сообщения о том, что внутриплевральная (ее также называют межплевральной) анальгезия (гл. 18) позволяет добиться полноценного обезболивания после торакотомии. К сожалению, на практике не всегда удается достичь удовлетворительных результатов, вероятнее всего из-за использования торакальных дренажей и наличия крови в плевральной полости.
^ Послеоперационные осложнения
Осложнения после торакотомии возникают достаточно часто, но в большинстве своем они незначительны и разрешаются без последствий. Густая мокрота и кровяные сгустки легко обтурируют просвет дыхательных путей, что вызывает ателектаз; лечение состоит в настойчивом, но аккуратном отсасывании мокроты. Массивный ателектаз после сегментарной puipi долевой резекции проявляется отклонением трахеи и смещением средостения в сторону оперированного легкого. При устойчивом
ателектазе, особенно в сочетании с вязкой густой мокротой, показана лечебная бронхоскошш.
Утечка воздуха часто происходит после резек-ЦР1Р1 легкого pis-за того, что долр! и сегменты в норме анатомически никогда полностью не отделяются щелями друг от друга; после резекции нередко остаются открытыми каналы, обеспечивающие коллатеральную вентиляцию. В подавляющем числе случаев утечка воздуха прекращается через несколько дней. Бронхоплевралъный свищ проявляется внезапным поступлением большого количества воздуха через плевральный дренаж, которое может сочетаться с прогрессирующим пневмотораксом и частичным коллапсом легкого. еслр! брон-хоплевральный свищ образуется в первые 24-72 ч после операции, то это обычно обусловлено неправильным наложением шва на культю бронха. Более позднее формирование бронхоплеврально-го свища вызвано некрозом бронхиального шва из-за ишемии или инфекции.
Некоторые осложнения встречаются редко, но заслуживают особого внимания, потому что они опасны для жизни, требуют высокой настороженности и часто служат показанием для неотложной диагностической торакотомии. Послеоперационное кровотечение обсуждалось выше. Если оперированное легкое чрезмерно расправляется, то может произойти скручивание доли или сегмента. Скручивание приводит к прекращению оттока крови по легочной вене из этой части легкого, что быстро вызывает кровохарканье и инфаркт легкого. Диагноз подтверждается гомогенным затемнением в границах сегмента или доли на рентгенограмме грудной клетки pi сдавлением извне соответствующего бронха при бронхоскопии. Острая дислокация сердца в оперированную половину грудной полости наблюдается в том случае, если после радикальной пульмонэктомии оставлен неушитым дефект в перикарде. Большой перепад давления между двумя половинами грудной полости вызывает это катастрофическое осложнение. Дислокация сердца в правую половину грудной полости приводит к внезапной тяжелой артериальной гипотонии и повышению ЦВД (из-за препятствия венозному притоку). При дислокации сердца в левую половину грудной полости происходит внезапное сдавление сердца на уровне предсердно-желудочковой борозды, что чревато артериальной гипотонией, ишемией и инфарктом миокарда. На рентгенограмме видно смещение tchpi сердца в оперированную половину грудной клетки.
Широкое рассечение средостенргя иногда приводит к повреждению диафрагмального, блуждающего и возвратного гортанного нервов. Послеопе-
рационный паралич диафрагмального нерва проявляется высоким стоянием ипсилатерального купола диафрагмы и трудностями при переводе пациента с ИВЛ на самостоятельное дыхание. При обширной резекции грудной стенки "en block" возникает патологическая подвижность грудной клетки (гл. 41), а если удаляют также и часть диафрагмы — то еще и вышеописанные трудности при переводе на самостоятельное дыхание. Параплегия — редкое осложнение после резекции легкого. Повреждение левых нижних межреберных артерий может сопровождаться ишемией спинного мозга (гл. 21). Если хирургический разрез распространяется на эпидуральное пространство, то может развиться эпидуральная гематома.
^ Резекция легких при определенных состояниях
Массивное легочное кровотечение
Массивное кровохарканье, объем которого превышает 500-600 мл за 24 ч, определяется как кровотечение из трахеобронхиального дерева. Это состояние осложняет только 1-2 % всех случаев кровохарканья и встречается при туберкулезе, бронхоэктазах, опухолях и после трансбронхиальной биопсии. Немедленное хирургическое вмешательство с резекцией легкого показано лишь при угрожающем жизни кровотечении. В большинстве случаев операция носит скорее "полуплановый", а не экстренный характер. Тем не менее послеоперационная летальность превышает 20 % (при консервативном лечении летальность составляет > 50 %). Можно попытаться эмболизовать поврежденные бронхиальные артерии. Наиболее частая причина смерти — асфиксия вследствие попадания крови в просвет дыхательных путей. Анестезия необходима при ригидной бронхоскопии, когда фибробронхоскопия не позволяет выявить источник кровотечения. Для тампонады используют бронхоблокатор или катетер Фогарти. Применяют лазерную коагуляцию (гл. 39).
Максимально долгое положение пациента на боку (пораженное легкое внизу) способствует остановке кровотечения. Следует установить несколько внутривенных катетеров большого диаметра. Бодрствующим пациентам во избежание усугубления гипоксии премедикацию седативны-ми препаратами не назначают; проводят ингаляцию 100 % кислорода. Если пациента интубирова-ли раньше и ему уже установлен бронхоблокатор, то для предотвращения кашля применяют седа-тивные препараты. До завершения резекции брон-
хоблокаторы оставляют на месте. Если интубаци-онная трубка еще не установлена, то предпочтительно проводить интубацию, когда пациент в сознании; но часто возникает необходимость в быстрой последовательной индукции (кетамин или этомидат и сукцинилхолин). При легочном кровотечении пациенты обычно проглатывают большое количество крови и поэтому рассматриваются как имеющие полный желудок; во время индукции анестезии им придают полусидячее положение и оказывают давление на перстневидный хрящ. Двухпросветная эндобронхиальная трубка крупного калибра идеально защищает здоровое легкое от крови и позволяет отсасывать содержимое из каждого легкого по отдельности. Если установка двухпросветной трубки технически сложна или ее узкие просветы быстро закупориваются, то устанавливают однопросветную трубку с внутренним диаметром не менее 8 мм, например однопросветную эндотрахеальную трубку с боковым каналом для бронхоблокатора (трубка "Юни-вент"). Введение раствора бикарбоната натрия облегчает отсасывание крупных кровяных сгустков из дыхательных путей.
^ Легочные кисты и буллы
Легочные кисты и буллы могут быть врожденными или приобретенными вследствие эмфиземы. Большие буллы препятствуют вентиляции, сдавливая окружающую легочную ткань. Механика этих воз-духосодержащих полостей часто такова, как если бы они имели однонаправленный впускной клапан, что приводит к прогрессивному возрастанию их объема. При нарастающей одышке или рецидивирующем пневмотораксе показана резекция легкого. Наиболее опасное интраоперационное осложнение анестезии — разрыв воздухосодержащей полости в период ИВЛ под положительным давлением. Это приводит к напряженному пневмотораксу. Разрыв может возникнуть с любой стороны еще до торакотомии или же в нижерасположенном (неоперируемом) легком во время резекции легкого. После индукции анестезии целесообразно сохранить самостоятельное дыхание пациента до тех пор, пока не будут установлены двухпросветная эндобронхиальная трубка или плевральный дренаж; у большинства пациентов увеличен объем мертвого пространства, поэтому во избежание чрезмерной гиперкапнии необходимо применить какой-либо режим вспомогательной вентиляции. Закись азота противопоказана, потому что она расширяет воздухосодержащие полости и вызывает их разрыв. Симптомы разрыва легочной кисты
или буллы: внезапная артериальная гипотония, бронхоспазм, резкое увеличение пикового давления на вдохе; лечение — немедленная установка плеврального дренажа.
^ Абсцесс легкого
Абсцесс легкого возникает в результате первичной легочной инфекции, при обструкции бронха опухолью или, в редких случаях, при гематогенном распространении системной инфекции. Необходимо как можно раньше разобщить легкие, чтобы не допустить попадания гноя из больного легкого в здоровое. Показана быстрая последовательная индукция неингаляционным анестетиком и эндобронхиальная интубация в положении пациента полусидя, причем пораженное легкое должно располагаться несколько ниже здорового, что предупреждает контаминацию последнего. Сразу же после установки эндобронхиальной трубки раздувают обе манжетки. Перед поворотом пациента набок необходимо убедиться, что бронхиальная манжетка раздута достаточно и защищает здоровое легкое от затека гноя. Во время операции нужно часто отсасывать отделяемое из бронха пораженного легкого.
^ Бронхоплевральный свищ
Бронхоплевральный свищ возникает после резекции легкого (чаще после пульмонэктомии), при прорыве абсцесса легкого в плевральную полость, при баротравме легкого и при спонтанном разрыве буллы. Если консервативное лечение (дренирование плевральной полости, антибактериальная терапия) не привело к положительному результату, показано оперативное вмешательство. Полноценная ИВЛ под положительным давлением невозможна из-за массивной утечки воздуха, риска развития напряженного пневмоторакса и распространения инфекции на другое легкое (при эмпиеме). В предоперационном периоде целесообразно максимально уменьшить объем эмпиемы и только потом закрывать бронхоплевральный свищ.
При значительной утечке воздуха иногда рекомендуют проводить интубацию двухпросветной эндобронхиальной трубкой на фоне сохраненного сознания. Альтернативный способ — быстрая последовательная индукция и интубация двухпросветной эндобронхиальной трубкой. Двухпросвет-ная эндобронхиальная трубка значительно упрощает выполнение анестезии, потому что позволяет изолировать свищ и осуществлять вентиляцию только здорового легкого. После операции необходимо экстубировать пациента как можно раньше.
^ Анестезия при резекции трахеи
Общие сведения
Показания к резекции трахеи включают стеноз и опухоли трахеи и, реже, некоторые врожденные заболевания. Стеноз трахеи возникает после закрытой или проникающей травмы, а также как осложнение интубации трахеи и трахеотомии. Большинство опухолей гистологически представляют собой плоскоклеточный рак и кистоз-ную аденокарциному. Сужение просвета трахеи вызывает прогрессирующую одышку. Физическая нагрузка может провоцировать свистящее дыхание и стридор. В положении лежа проходимость дыхательных путей часто ухудшается и одышка становится более выраженной. При опухолях трахеи может возникать кровохарканье. KT помогает уточнить локализацию патологического процесса. Измерение петли "поток-объем" позволяет определить анатомический уровень и выраженность обструкции дыхательных путей (рис. 24-10).
Анестезия
У абсолютного большинства пациентов имеется среднетяжелая или тяжелая обструкция дыхательных путей, поэтому премедикацию не назначают или применяют низкие дозы препаратов. Использование м-холиноблокаторов — противоречивый вопрос, потому что теоретически они вызывают неблагоприятное повышение вязкости секрета желез дыхательных путей. Необходим ин-вазивный мониторинг АД; при резекции нижней части трахеи, когда высок риск сдавления безымянной артерии, целесообразно катетеризировать левую лучевую артерию.
При тяжелой обструкции дыхательных путей для индукции анестезии использует ингаляционный анестетик (F1O2 100 %). Концентрацию анестетика во вдыхаемой смеси повышают постепенно. Препаратом выбора считается галотан, потому что он обладает наименьшим раздражающим действием и слабее подавляет дыхание, чем другие ингаляционные анестетики (гл. 7). Во время индукции анестезии больной должен дышать самостоятельно. Миорелаксанты применять нельзя, потому что расслабление мышц способно вызвать полную обструкцию дыхательных путей. Ларингоскопию выполняют только по достижении достаточно глубокого уровня анестезии. Лидокаин (1-2 мг/кг в/в) углубляет анестезию без подавления дыхания. Далее хирург mo-
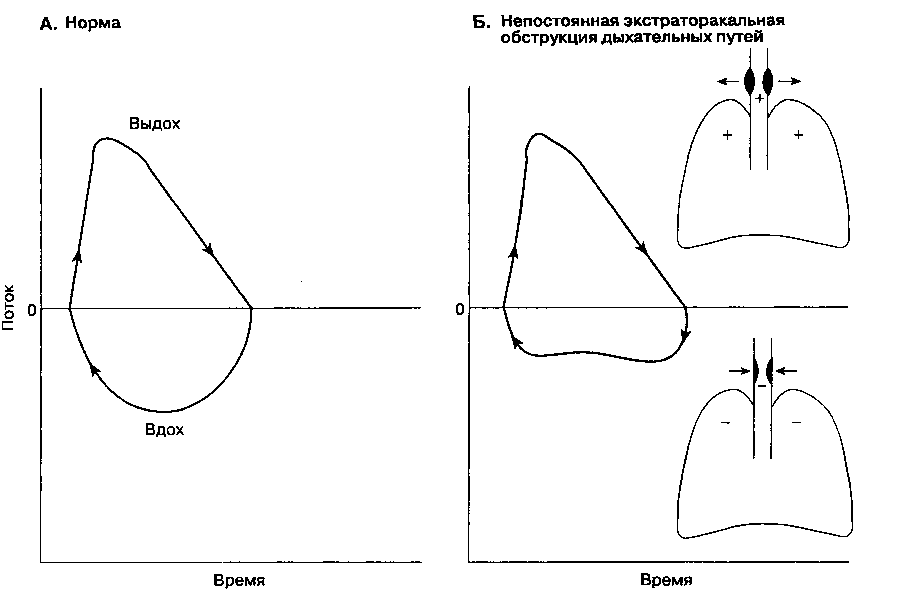
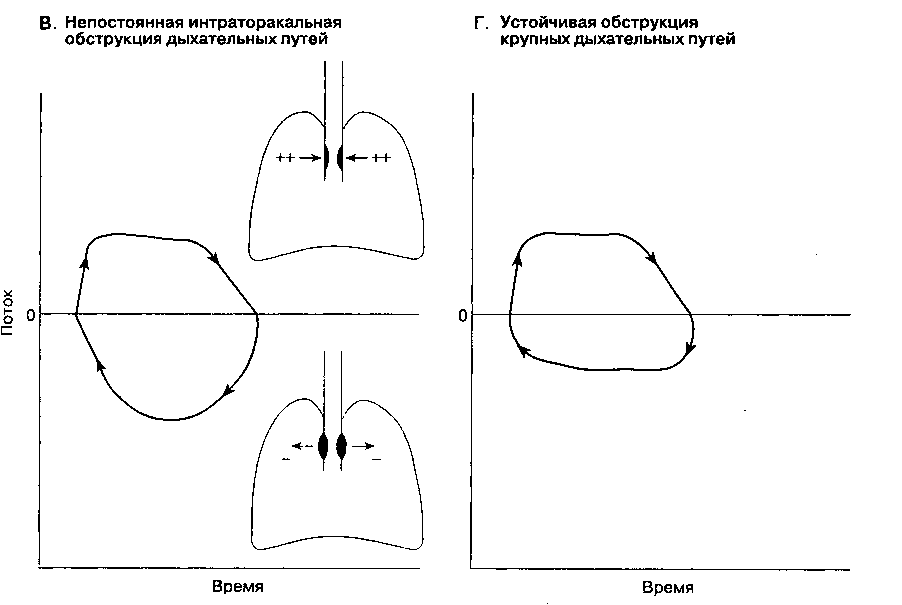
Рис. 24-10. Петли "поток-объем"

Рис. 24-11. Поддержание проходимости дыхательных путей при операциях на проксимальной части трахеи
жет выполнить ригидную бронхоскопию для оценки характера патологического процесса и дилатации трахеи. После бронхоскопии выполняют интубацию трахеи трубкой малого диаметра, чтобы ее можно было провести дистальнее места обструкции.
При вмешательствах на проксимальной части трахеи используют воротникообразный разрез на шее. После пересечения трахеи в дистальный отрезок вводят стерильную армированную трубку, к которой на время резекции подключают аппарат ИВЛ. После резекции и наложения задней дуги ре-анастомоза армированную трубку извлекают, а эн-дотрахеальную трубку продвигают дистальнее линии анастомоза (рис. 24-11). Альтернативный способ вентиляции во время наложения анастомоза — струйная ВЧ ИВЛ, когда катетер ВЧ-респира-тора продвигают за место обструкции в дистальный отрезок трахеи (рис. 24-12). Сразу после операции целесообразно перевести пациента на самостоятельное дыхание и экстубировать. В раннем послеоперационном периоде для создания нужного наклона под голову пациента кладут подушку, что ослабляет натяжение швов реанастомоза (рис. 24-13).
При вмешательствах на дистальной части трахеи прибегают к стернотомии или правосторонней задней торакотомии. Принципы анестезии сходны с описанными для операций на проксимальной части, но необходимость в привлечении технически сложных методик (струйная ВЧ ИВЛ, искусственное кровообращение) возникает чаще.
