Книга вторая Дж. Эдвард Морган-мл. Мэгид С. Михаил Перевод с английского
| Вид материала | Книга |
- Книга первая Дж. Эдвард Морган-мл. Мэгид С. Михаил Перевод с английского, 10010.77kb.
- А. Конан-Дойль новоеоткровени е перевод с английского Йога Рàманантáты, 2314.23kb.
- Copyright Сергей Александровский, перевод с английского Email: navegante[a]rambler, 619.61kb.
- "книга непрестанности осириса " 177, 7373.41kb.
- Н. М. Макарова Перевод с английского и редакция, 4147.65kb.
- Трудового Красного Знамени гупп детская книга, 2911.61kb.
- Трудового Красного Знамени гупп детская книга, 2911.77kb.
- Уайнхолд Б., Уайнхолд Дж. У 67 Освобождение от созависимости / Перевод с английского, 11462.2kb.
- Малиновской Софьи Борисовны Специальность: журналистика Специализация: художественный, 969.08kb.
- Духовные истины в психических явлениях перевод с английского 3-е издание Москва «Философская, 1557.75kb.
Опухоли легких могут быть доброкачественными, злокачественными или занимать промежуточное положение. Лишь в редких случаях удается составить мнение о характере опухоли до операции. На гамартомы приходится 90 % доброкачественных опухолей легких. Они располагаются в периферических отделах легкого и образованы дезорганизованной нормальной легочной тканью. Аденомы чаще возникают в крупных бронхах, носят, как правило, доброкачественный характер,
но иногда способны к локальному инвазивному росту, а в редких случаях даже метастазируют. Аденомы бронхов включают карциноидные опухоли, цилиндромы и мукоэпидермоидные аденомы. Они часто обтурируют просвет бронха и вызывают рецидивирующую пневмонию дистальнее места обструкции. Карциноидные опухоли образуется из клеток APUD-системы и могут секретировать различные гормоны, включая АКТГ и аргинин-ва-зопрессин; клинические проявления карциноид-ного синдрома наблюдаются редко и чаще всего возникают при метастазах в печень (гл. 36).
Злокачественные опухоли легких подразделяют на две большие группы: мелкоклеточный рак (синоним — овсяноклеточный рак) и немелкокле-точный рак. Немелкоклеточный рак включает плоскоклеточный рак, аденокарциному и крупноклеточный рак (синоним — анапластическая карцинома). Все виды рака легкого чаще всего отмечаются у курильщиков, но аденокарцинома встречается и у некурящих. Плоско- и мелкоклеточный рак чаще поражает крупные бронхи, тогда как аденокарцинома и крупноклеточный рак — периферические отделы легкого с распространением на плевру.
^ Клиническая картина
Симптомы: кашель, кровохарканье, одышка, свистящее дыхание, потеря веса, лихорадка и отхожде-ние мокроты. Последние два симптома обусловлены пневмонией в результате обструкции бронха. Плевритическая боль в груди и плевральный выпот указывают на поражение плевры. О поражении средостения свидетельствует ряд симптомов: охриплость голоса из-за сдавления возвратного гортанного нерва, симптом Горнера при вовлечении симпатического ствола (гл. 18), высокое стояние купола диафрагмы при сдавлении диаф-рагмального нерва, дисфагия при сдавлении пищевода, синдром верхней полой вены. При поражении сердца развиваются выпотной перикардит и кардиомегалия. При опухолях верхушки легкого (верхней борозды) с распространением на корешки C7-T2 появляются боли в надплечье и руке (синдром Пенкоста). Отдаленные метастазы поражают головной мозг, кости, печень и надпочечники.
Опухоли легких, особенно мелкоклеточный рак, могут вызывать симптоматику, не связанную с их анатомической локализацией,— так называемые паранеопластические синдромы. Механизмы этого явления включают эктопическую выработку гормонов и перекрестные иммунологические реакции между опухолью и нормальной тканью. У пациентов могут наблюдаться синдром Кушинга, гипо-
натриемия и гиперкальциемия, которые обусловлены секрецией АКТГ, аргинин-вазопрессина и па-ратгормона соответственно (гл. 36). Синдром Итона-Ламберта — разновидность миастении — характеризуется миопатией проксимальных групп мышц, причем сила мышц возрастает при повторных попытках сокращения (что не свойственно ту asthenia gravis; гл. 37). К прочим паранеопласти-ческим синдромам относятся гипертрофическая остеоартропатия, дегенерация мозжечка, периферическая нейропатия, полимиозит, мигрирующий тромбофлебит и асептический эндокардит.
Лечение
Лучший метод лечения курабельных случаев рака легкого — хирургическое вмешательство. Резекция показана при немелкоклеточном раке в отсутствие выраженного поражения лимфоузлов, вовлечения средостения и отдаленных метастазов. При мелкоклеточном раке легкого хирургическое лечение неэффективно, потому что к моменту установления диагноза опухоль практически всегда метастазирует; лечение состоит в проведении химиотерапии и лучевой терапии.
^ Резектабельность и операбельность. Резекта-бельность определяется стадией опухоли, а операбельность зависит от объема операции и общего состояния пациента. Определение стадии опухоли включает рентгенографию грудной клетки, KT, бронхоскопию и медиастиноскопию. При метастазах в ипсилатеральные бронхиальные лимфоузлы и ипсилатеральные лимфоузлы ворот легкого опухоль считается резектабельной. При метастазах в ипсилатеральные медиастинальные или ипсилатеральные нижние трахеобронхиальные узлы опухоль можно удалить уже не всегда. При метастазах в лестничные, надключичные, контралатеральные медиастинальные лимфоузлы или контралатеральные лимфоузлы ворот легкого опухоль нерезекта-бельна. При опухолях, поражающих грудную стенку, в отсутствие медиастинальных метастазов в некоторых клиниках выполняют резекцию uen block"; сходную операцию проводят после лучевой терапии при опухоли верхушки легкого в отсутствие метастазов в медиастинальные лимфоузлы.
Анатомические границы резекции должны быть достаточно велики для адекватной эрадика-ции опухоли, а объема оставшейся паренхимы должно хватить для полноценной легочной функции в послеоперационном периоде. Лобэктомия, выполненная через задний доступ в 5-м или 6-м меж-реберье,— это операция выбора при большинстве опухолей легкого. Сегментарные или клиновидные резекции показаны при небольших перифери-
ческих опухолях, а также при значительно сниженном функциональном легочном резерве. Пульмонэктомия показана при поражении левого или правого главного бронха, а также при распространении опухоли до ворот легкого. Функциональные критерии пульмонэктомии рассматриваются ниже. При поражении проксимальных участков бронхов на фоне сниженного функционального легочного резерва альтернативой пульмонэктомии является циркулярная резекция; при этом удаляют пораженный долевой бронх вместе с частью правого или левого главного бронха, после чего накладывают анастомоз между дистальным отрезком главного бронха и проксимальным отрезком или трахеей. При опухолях трахеи возможна циркулярная пульмонэктомия. Летальность после пульмонэктомии составляет 5-6 %, после лобэкто-мии — 2-3%. При пульмонэктомии правого легкого летальность выше, возможно из-за потери большего объема ткани (по сравнению с левосторонней пульмонэктомией). Послеоперационная летальность преимущественно обусловлена сердечно-сосудистыми осложнениями.
^ Функциональные критерии пульмонэктомии
Мнение об операбельное™ составляют на основе клинической оценки, однако исследование функции легких позволяет получить очень важную информацию. Выраженность дисфункции легких прямо пропорциональна риску операции. Стандартные критерии операбельности легких представлены в табл. 24-4. Если показатели пациента не соот-
^ ТАБЛИЦА 24-4. Исследование функции дыхания перед пульмонэктомией: критерии операбельности
| Тест | Результат, соответствующий высокому риску осложнений |
| Газы артериаль- | PaCO2 > 45 мм рт. ст. (при дыхании |
| ной крови | атмосферным воздухом) |
| 0OB1 | <2л |
| ОФВ,/ФЖЕЛ | < 50 % от должной величины |
| Максимальная | < 50 % от должной величины |
| дыхательная | |
| емкость | |
| ОО/ОЕЛ | > 50 % от должной величины |
| Максимальное | < 10 мл/кг/мин |
| потребление | |
| кислорода (VO2) | |
| DUo (диффузион- | < 40 % от должной величины |
| ная способность | |
| легких по СО) | |
ветствуют любому из этих критериев, проводят раздельное исследование функции каждого легкого. ^ Считается, что опухоль операбельна, если предсказанный послеоперационный 00B1 > 800 мл. Удельный вклад каждого легкого в общий QOB1 пропорционален проценту общего легочного кро-вотока, который получает это легкое. Легочный кровоток измеряют при радиоизотопном сканировании (133Xe или 99Tc).
Послеоперационный QOB1 =
= % легочного кровотока х общий 00B1.
Удаление значительно пораженного легкого (вентиляция отсутствует, но перфузия сохранена) не оказывает неблагоприятного влияния на легочную функцию и даже может улучшить оксигена-цию. Если предсказанный послеоперационный GOB1 < 800 мл, но пульмонэктомия по-прежнему необходима, то нужно проверить способность сосудов здорового легкого приспособиться к объему общего легочного кровотока. Для этого выполняют ангиопульмонографию: главную легочную артерию пораженного легкого перекрывают с помощью баллона-катетера: при ДЛАср > 40 мм рт. ст. или PaO2 < 45 мм рт. ст., пациент не перенесет пульмон-эктомию.
Максимальное потребление кислорода (VO2) — важный прогностический фактор осложнений и летальности в послеоперационном периоде. Если VO2 > 20 мл/кг/мин, то риск осложнений низок. Если VO2 < 10 мл/кг/мин, то риск осложнений неприемлемо высок.
^ 2. ЛЕГОЧНЫЕ ИНФЕКЦИИ
Легочная инфекция может быть в виде одиночного узла или же абсцесса (некротизирующий пнев-монит). Диагностическая торакотомия показана для исключения злокачественной опухоли и определения возбудителя. Абсцесс легкого, резистент-ный к антибактериальной терапии, или сочетан-ный с рефрактерной эмпиемой, или вызывающий тяжелое кровохарканье,— показание к резекции легкого. Легочную инфекцию вызывают бактерии (анаэробы, Mycoplasma, Mycobacterium tuberculosis, Nocardia, различные кишечные и некишечные гноеродные микроорганизмы) и грибы (Histo-plasma, Coccidioides, Cryptococcus, Blastomyces, Мисог и Aspergillus).
3. БРОНХОЭКТАЗЫ
Бронхоэктазы представляют собой постоянно расширенные бронхи. Обычно бронхоэктазы являются конечным результатом тяжелого или рецидиви-
рующего воспаления pi обструкции бронхов. Причины: вирусные, бактериальные и грибковые инфекции, вдыхание токсичных газов, аспирация желудочного содержимого, нарушение мукоцили-арного клиренса (при муковисцидозе или дисфункции реснитчатого эпителия). Бронхиальные мышцы и эластичные волокна замещаются богато васкуляризованной рубцовой тканью, что вызывает приступы кровохарканья. Резекция легкого показана при массивном кровохарканье, когда консервативное лечение неэффективно, а бронхо-эктазы расположены локально. При диффузных бронхоэктазах развивается выраженное нарушение вентиляции по обструктивному типу (гл. 23).
Анестезия
^ 1. ПРЕДОПЕРАЦИОННЫЙ ПЕРИОД
Предоперационная подготовка пациентов с сопутствующими заболеваниями легких детально обсуждается в гл. 23. Курение является фактором риска возникновенияХОЗЛиИБС(гл. 20), которые часто сопутствуют хирургической легочной патологии. Эхокардиография позволяет оценить функцию сердца, а также обнаружить увеличение и гипертрофию ПЖ (cor pulmonale). Для диагностики ИБС можно использовать стресс-эхокардиогра-фию с добутамином (гл. 20).
При онкологических заболеваниях выявляют изменения, обусловленные анатомическим распространением опухоли и паранеопластическими синдромами. Тщательно исследуют рентгенограммы и компьютерные томограммы грудной клетки. Смещение трахеи и бронхов осложняет интубацию трахеи и правильную установку эндобронхи-альной трубки. Сдавление дыхательных путей затрудняет масочную вентиляцию при индукции анестезии. Обширные легочные инфильтраты, ателектазы и массивный плевральный выпот значительно повышают риск возникновения гипоксемии. Отмечают локализацию буллезных кист и абсцессов.
^ После торакальных операций высок риск развития легочных осложнений (гл. 23). Правильная предоперационная подготовка помогает снизить их частоту. При сердечной недостаточности или наджелудочковых тахикардиях в предоперационном периоде назначают сердечные гликозиды. Аритмии, особенно наджелудочковые тахикардии, могут быть вызваны хирургическими манипуляциями или растяжением правого предсердия при редукции легочной сосудистой сети. Частота аритмий увеличивается с возрастом и зависит от объема резекции.
Премедикация
При среднетяжелой и тяжелой дыхательной недостаточности дозу седативных препаратов снижают или их вообще исключают из премедикации. Хотя м-холиноблокаторы (атропин, 0,5 мг в/м, или гли-копирролат, 0,2 мг в/м) теоретически повышают вязкость секретов экзокринных желез и увеличивают мертвое пространство, на практике они чрезвычайно эффективно подавляют избыточную секрецию, улучшая визуализацию дыхательных путей при повторных ларингоскопиях и облегчая применение фибробронхоскопа.
^ 2. ИНТРАОПЕРАЦИОННЫЙ ПЕРИОД Подготовка
Как и в кардиохирургии, правильная подготовка позволяет избежать катастрофических осложнений. Низкий функциональный легочный резерв, анатомические аномалии, сдавление дыхательных путей, однолегочная вентиляция — все это повышает риск гипоксемии. Необходимо иметь четкий и хорошо продуманный план на случай возникновения всех возможных осложнений. Более того, помимо обязательного набора для обеспечения проходимости дыхательных путей (гл. 5), нужно иметь готовое к работе дополнительное оборудование: несколько одно- и двухпросветных трубок разных размеров, фибробронхоскоп, "трубкообменник" малого диаметра, приспособление для вспомогательной вентиляции в режиме постоянного положительного давления в дыхательных путях (ППДДП) и адаптер для ингаляции бронходилата-торов в дыхательный контур наркозного аппарата. Если в послеоперационном периоде планируют эпидуральную анальгезию, то целесообразно установить катетер перед индукцией анестезии. Объяснение пациенту хода выполнения этапов анестезии облегчает правильную установку катетера и снижает частоту неврологических осложнений.
^ Венозный доступ
При торакальных операциях необходимо установить минимум один в/в катетер большого диаметра (14-16 G). Если прогнозируется масивная кровопо-теря, целесообразно катетеризировать центральную вену (на стороне операции), подготовить приспособления для согревания крови и быстрой инфузии.
Мониторинг
Показания к инвазивному мониторингу АД: одно-легочная вентиляция, резекция обширных опухолей (особенно распространяющихся в средостение
или на грудную стенку), тяжелая дыхательная недостаточность, тяжелое сердечно-сосудистое заболевание. Мониторинг ЦВД показан при пульмо-нэктомии и при резекции больших опухолей. ЦВД отражает изменения венозной емкости, ОЦК и функции ПЖ, поэтому мониторинг ЦВД позволяет только ориентировочно оценить состояние ге-модинамики. При легочной гипертензии, легочном сердце и дисфункции ЛЖ показана катетеризация легочной артерии; после установки катетера необходимо выполнить рентгенографию грудной клетки, чтобы исключить его случайное попадание в удаляемый сегмент легкого. Если кончик катетера находится в легочной артерии коллабирован-ного оперируемого легкого, то при однолегочной вентиляции показатели сердечного выброса и напряжения кислорода в смешанной венозной крови будут занижены. После пулъмонэктомии баллон катетер а раздувать нельзя, потому что общее поперечное сечение оставшихся легочных сосудов значительно снижено и раздувание баллона резко повышает постнагрузку ПЖ и может уменьшать преднагрузку ЛЖ.
^ Индукция анестезии
После адекватной предварительной оксигенации проводят индукцию анестезии барбитуратами. Выбор анестетика зависит от общего состояния пациента. Для предотвращения рефлекторного брон-хоспазма и прессорной реакции на прямую ларингоскопию следует ввести дополнительную дозу индукционного анестетика и/или наркотический анальгетик непосредственно перед интубацией (гл. 20). При повышенных рефлексах с дыхательных путей целесообразно углубить анестезию ингаляционным анестетиком.
Сукцинилхолин или недеполяризующий мио-релаксант облегчают интубацию трахеи. Если ожидается трудная интубация, то лучше использовать сукцинилхолин. Для большинства торакотомий достаточно стандартной эндотрахеальной интуба-
ции, но в некоторых случаях однолегочная вентиляция значительно облегчает выполнение операции. Однопросветную эндотрахеальную трубку устанавливают в том случае, если перед операцией хирургу нужно провести диагностическую бронхоскопию; после бронхоскопии ее меняют на двух-просветную эндобронхиальную трубку. Управляемая ИВЛ предупреждает появление ателектазов, парадоксального дыхания и смещения средостения, а также облегчает манипуляции на легком.
^ Положение пациента на операционном столе
После индукции анестезии, интубации и подтверждения правильного положения эндотрахеальной или эндобронхиальной трубки устанавливают дополнительные в/в катетеры и линии мониторинга, а затем пациенту придают определенное положение. Большинство резекций легкого выполняют через задний доступ в положении пациента на боку. Необходимо правильно уложить пациента, чтобы избежать травматических сдавлений и облегчить оперативный доступ. Нижерасположенную руку сгибают, тогда как вышерасположенную размещают перед головой так, чтобы лопатка сместилась в сторону от места операции (рис. 24-9). Между руками и ногами прокладывают подушечки; для профилактики травмы плечевого сплетения обязательно подкладывают подмышечный валик. Следует избегать давления на глаза и нижерасположенное ухо.
^ Поддержание анестезии
В торакальной хирургии применяют все современные методики анестезии, но наибольшее распространение получило сочетание мощных га-логенированных ингаляционных анестетиков (галотан, энфлюран, изофлюран, севофлюран и десфлюран) с наркотическим анальгетиком. Преимуществами ингаляционных анестетиков являются: (1) мощная дозозависимая бронходилата-
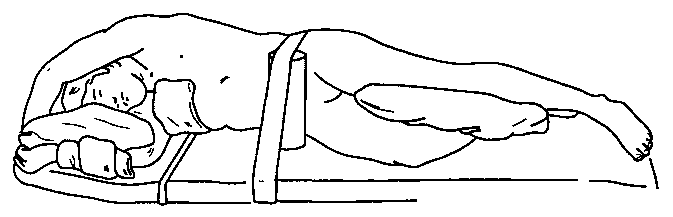
Рис. 24-9. Латеральная торакотомия: правильное положение пациента на операционном столе. (С разрешения. Из: Gothard J. W. W., Branthwaite M. A. Anaesthesia for Thoracic Surgery. Blackwell, 1982.)
ция; (2) подавление рефлексов с дыхательных путей; (3) возможность использовать высокую FiO2; (4) легкая управляемость глубиной анестезии; (5) незначительное влияние на гипоксичес-кую легочную вазоконстрикцию. В дозе < 1 МАК галогенированные ингаляционные анестетики практически не подавляют гипоксическую легочную вазоконстрикцию (гл. 22). К преимуществам наркотических анальгетиков относятся: (1) незначительное влияние на гемодинамику; (2) подавление рефлексов с дыхательных путей); (3) остаточная послеоперационная анальгезия. Если для послеоперационной анальгезии планируется эпиду-ралъное введение наркотических анальгетиков, то во избежание депрессии дыхания следует минимизировать их в/в введение во время операции. Ингаляция закиси азота влечет за собой значительное снижение FiO2, поэтому ее применение не рекомендовано. Как и галогенированные ингаляционные анестетики, закись азота подавляет гипоксическую легочную вазоконстрикцию, а в ряде случаев провоцирует развитие легочной гипер-тензии.
Недеполяризующие миорелаксанты облегчают как ретракцию ребер, так pi ведение анестезии. В процессе расширения межреберного промежутка необходима максимальная глубина анестезии. Устойчивую брадикардию, обусловленную раздражением блуждающего нерва при хирургических манипуляциях, устраняют введением атропина в/в. При негерметичной грудной клетке венозный возврат уменьшается, потому что на стороне операции присасывающее действие отрицательного внутригрудного давления отсутствует. Струйная инфузия жидкости увеличивает венозный возврат.
^ При резекции легкого необходимо строго ограничивать инфузию жидкости, восполнять только ба-зальные потребности организма в жидкости и кро-вопотерю (гл. 29). Для восполнения кровопотери используют коллоиды и препараты крови. Инфузия чрезмерного количества жидкости в положении пациента на боку может вызвать "синдром нижерасположенного легкого", когда под действием силы тяжести жидкость накапливается в нижерасположенном легком. Это увеличивает внутриле-гочный шунт pi приводит к гипоксемии, особенно при однолегочной вентиляции. Более того, после расправления в оперированном легком ppick развития отека также достаточно высок.
В ходе операции на бронх (или оставшуюся легочную ткань) накладывают швы с помощью специального устройства, после чего культю бронха проверяют на герметичность под водой (для этого
кратковременно поднимают давление в дыхательных путях до 30 см вод. ст.). Если при резекции легкого проводили обычную, а не однолегочную ИВЛ (т. е. оперируемое легкое не спадалось), то при сопоставлении ребер во избежание травмирования легочной паренхимы хирургической иглой целесообразно перейти на ручную вентиляцию дыхательным мешком. Перед закрытием грудной полости вручную полностью расправляют все сегменты легкого под контролем зрения, после чего снова переходят на принудительную ИВЛ, которую необходимо продолжать до подсоединения плевральных дренажей к отсосу. После пульмонэктомии плевральные дренажи не устанавлртвают.
