Книга вторая Дж. Эдвард Морган-мл. Мэгид С. Михаил Перевод с английского
| Вид материала | Книга |
- Книга первая Дж. Эдвард Морган-мл. Мэгид С. Михаил Перевод с английского, 10010.77kb.
- А. Конан-Дойль новоеоткровени е перевод с английского Йога Рàманантáты, 2314.23kb.
- Copyright Сергей Александровский, перевод с английского Email: navegante[a]rambler, 619.61kb.
- "книга непрестанности осириса " 177, 7373.41kb.
- Н. М. Макарова Перевод с английского и редакция, 4147.65kb.
- Трудового Красного Знамени гупп детская книга, 2911.61kb.
- Трудового Красного Знамени гупп детская книга, 2911.77kb.
- Уайнхолд Б., Уайнхолд Дж. У 67 Освобождение от созависимости / Перевод с английского, 11462.2kb.
- Малиновской Софьи Борисовны Специальность: журналистика Специализация: художественный, 969.08kb.
- Духовные истины в психических явлениях перевод с английского 3-е издание Москва «Философская, 1557.75kb.
Конечная порция выдыхаемого газа практически представляет собой альвеолярный газ, а РлСО2 фактически идентична PaCO2, поэтому напряжение CO2 в конечной порции выдыхаемого газа, РктСО2, используется клинически для оценки PaCO2 (гл. 6). Разница между РлСО2 и РктСО2 в норме не превышает 5 мм рт. ст. и обусловлена разведением альвеолярного газа газом из неперфузи-руемых альвеол, не содержащим CO2 (т. е. газом из альвеолярного мертвого пространства).
^ Транспорт дыхательных газов в крови
1. КИСЛОРОД
Кислород переносится кровью в растворенном виде и в связанной (обратимо) с гемоглобином форме.
^ Физически растворенный кислород
Количество кислорода, растворенного в крови, определяется законом Генри, согласно которому концентрация любого газа в растворе пропорцио-
нальна его парциальному давлению. Математическое выражение этого закона следующее:
Концентрация газа = а х Парциальное давление,
где а — коэффициент растворимости газа в данном растворе и при данной температуре.
Коэффициент растворимости кислорода в крови при нормальной температуре тела равен 0,003 мл/100 мл/мм рт. ст. Даже при РлО?, равном 100 мм рт. ст., максимальное количество кислорода, которое может раствориться в крови, очень мало (0,3 мл в 100 мл крови) по сравнению с фракцией кислорода, связанного с гемоглобином.
Гемоглобин
Гемоглобин — это крупная сложная молекула, состоящая из четырех железосодержащих порфири-новых соединений (гемов) и четырех белковых субъединиц. Железо, которое содержится в теме, играет главную роль в образовании связи с кислородом; с кислородом может связываться только двухвалентная форма железа. В норме у взрослых имеется так называемый гемоглобин A1, состоящий из двух а- и двух (3-цепей (субъединиц); эти четыре цепи удерживаются вместе за счет слабых связей между аминокислотными остатками. Теоретически каждый грамм гемоглобина способен переносить до 1,39 мл кислорода.
^ Кривая диссоциации оксигемоглобина
Молекула гемоглобина присоединяет четыре молекулы кислорода. В результате сложного взаимодействия между субъединицами связывание гемоглобина с кислородом носит нелинейный характер (соответствующая кривая зависимости имеет S-образную форму; рис. 22-22). Насыщением (сатурацией) гемоглобина называют количество связанного с гемоглобином кислорода, отнесенное к общей кислородной емкости гемоглобина и выраженное в процентах. Присоединение каждой из четырех молекул кислорода обеспечивается отдельной химической реакцией. Изменение молекулярной кон-формации гемоглобина, возникающее в результате присоединения первых трех молекул кислорода, резко ускоряет образование четвертой связи с кислородом. Последняя реакция отвечает за ускоренное присоединение кислорода в диапазоне насыщения от 25 до 100 %. В диапазоне от 90 до 100 % кривая диссоциации (насыщения) постепенно уплощается по мере уменьшения количества доступных мест связывания кислорода.
^ Факторы, влияющие на кривую диссоциации оксигемоглобина
На процесс присоединения кислорода к гемоглобину влияют следующие факторы: концентрация ионов водорода, напряжение углекислого газа, температура, концентрация 2,3-дифосфоглице-рата (2,3-ДФГ). Их суммарный эффект на взаимодействие гемоглобина с кислородом отражает величина P50 — значение напряжения кислорода, при котором гемоглобин насыщен на 50% (рис. 22-23). Изменение каждого из факторов способно смещать кривую диссоциации вправо (увеличение P50) или влево (уменьшение Р.™). Сдвиг вправо вызывает снижение сродства гемоглобина к кислороду, вытесняет кислород из связи с гемоглобином и увеличивает количество кислорода, доступного тканям; сдвиг влево дает обратный эффект. В норме P50 составляет 26,6 мм рт. ст. (3,4 кПа).
Увеличение концентрации ионов водорода в крови снижает связывание гемоглобина с кислородом (эффект Бора). Форма кривой диссоциации оксигемоглобина такова, что этот эффект более выражен в венозной крови, чем в артериальной (рис. 22-23); данный феномен облегчает осво-
бождение кислорода в тканях, практически не сказываясь на потреблении кислорода (в отсутствие тяжелой гипоксии).
Влияние напряжения CO2 на сродство гемоглобина к кислороду имеет важное физиологическое значение; вместе с тем оно вторично по отношению к увеличению концентрации ионов водорода, которая возрастает с увеличением PCO2. Высокое содержание CO2 в венозном сегменте капилляров, снижая сродство гемоглобина к кислороду, облегчает освобождение кислорода в тканях; наоборот, низкое содержание CO2 в легочных капиллярах вновь увеличивает сродство гемоглобина к кислороду, облегчая поглощение кислорода из альвеол.
2,3-ДФГ, побочный продукт гликолиза (шунт Rapoport-Luebering), накапливается при анаэробном метаболизме. Хотя эффект 2,3-ДФГ на гемоглобин теоретически благоприятен для организма (уменьшается сродство гемоглобина к кислороду и облегчается освобождение O2 в тканях.— Примеч. ред.), его физиологическое значение невелико. 2,3-ДФГ, тем не менее, играет важную компенсаторную роль при хронической анемии и существенно влияет на транспортную функцию гемоглобина донорской крови при гемотрансфузиях (гл. 29).
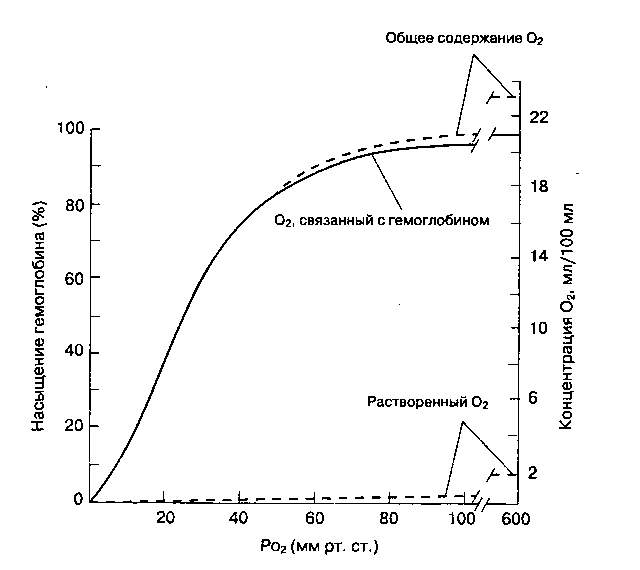
Рис. 22-22. Кривая диссоциации оксигемоглобина у здорового взрослого человека. (С разрешения. Из: West J. В. Respiratory Physiology: The Essentials, 3rd ed. Williams & Wilkins, 1985.)
^ Аномальные лиганды и аномальные формы гемоглобина
Окись углерода (СО), цианиды, азотная кислота и аммиак moitt связываться с гемоглобином в местах соединения с кислородом. Они вытесняют кислород и смещают кривую диссоциации влево. Угарный газ отличается особенной активностью: его сродство к гемоглобину в 200-300раз выше, чем у кислорода. СО связывается с гемоглобином, образуя карбоксигемоглобин, что снижает кислородную емкость гемоглобина и нарушает освобождение кислорода в тканях.
При окислении железа тема до трехвалентной формы образуется метгемоглобин. В редких случаях нитраты, нитриты, сульфаниламиды и другие лекарственные средства могут вызывать сильную метгемоглобинемию. Метгемоглобин неспособен связывать кислород, до тех пор пока он не будет восстановлен с помощью фермента метгемо-глобинредуктазы; кроме того, метгемоглобин смещает кривую диссоциации оксигемоглобина влево. Метгемоглобинемия, как и отравление угарным газом, снижает кислородную емкость крови и нарушает высвобождение кислорода в тканях. Метилено-вый синий и аскорбиновая кислота способствуют восстановлению метгемоглобина в гемоглобин.
Аномальные формы гемоглобина возникают в результате изменений в составе белковых субъединиц. Каждый вариант имеет собственные характеристики связывания с кислородом. Наиболее распространенные аномальные формы гемоглобина включают фе-тальный гемоглобин, гемоглобин A2, гемоглобин при серповидно-клеточной анемии (гл. 29).
^ Содержание кислорода в крови
Общее содержание кислорода в крови равно сумме физически растворенного и связанного с гемоглобином кислорода. Связывание кислорода с гемоглобином никогда не достигает теоретического максимума, поэтому считают, что 1 г гемоглобина может связать приблизительно 1,31 мл кислорода. Содержание кислорода в крови (С, от англ, content — содержание) выражается следующим уравнением:
Содержание кислорода (в 100 мл крови) = = [(0,003 мл О2/ЮО мл крови/мм рт. ст.) х PO2] + + (SO2X HbX 1,31 мл/1 OO мл крови),
где Hb — концентрация гемоглобина (г/100 мл крови), a SO2 — насыщение гемоглобина кислородом (S, от англ, saturation — насыщенеие) при данном PO2.
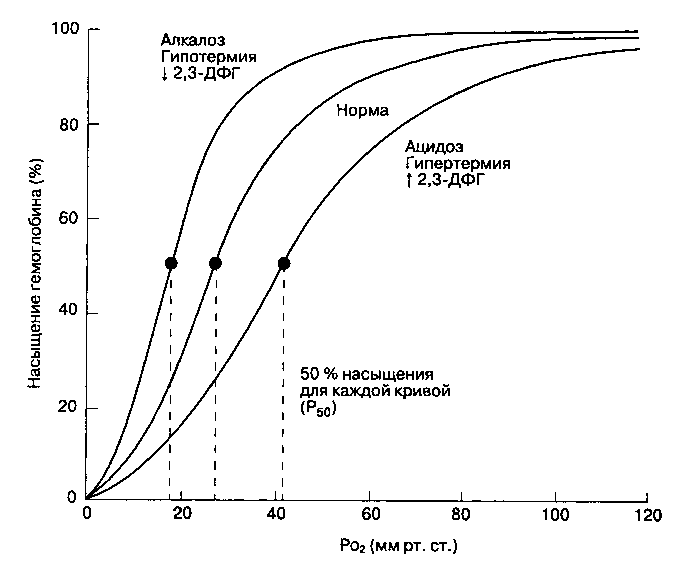
Рис. 22-23. Сдвиги кривой диссоциации оксигемоглобина при изменениях рН, температуры тела и концентрации 2,3-дифосфоглицерата (2,3-ДФГ) в эритроцитах
Используя эту формулу и величину Hb, равную 15 г/100 мл, можно рассчитать содержание O2 в артериальной pi смешанной венозной крови, а также артериовенозную разницу по кислороду (при SaO2 - 97,5 % и SvO2 = 75 %):
CaO2-(O1OOSx 100)+ (0,975 х 15 х 1,31)=
= 19,5 мл О2/100 мл крови;
CvO2-(0,003 х 40)+ (0,75 х 15 х 1,31) =
- 14,8 мл О2/100 мл крови;
(CaO2 - CvO2) - 4,7 мл О2/1OO мл крови.
^ Транспорт кислорода
Транспорт кислорода зависит как от дыхания, так и от кровообращения (гл. 19). Общая доставка кислорода (DO2; от англ, delivery — доставка) к тканям равна произведению содержания кислорода в артериальной крови и сердечного выброса:
DO2 - CaO2 х Qt.
Заметим, что содержание кислорода в артериальной крови зависит как от РлО2, так и от концентрации гемоглобина. ^ Следовательно, недостаточная доставка кислорода может быть результатом низкого РлО2, низкой концентрации гемоглобина или низкого сердечного выброса. В норме расчет доставки кислорода выглядит так:
DO2 = 20 мл О2/1OO мл крови х 5000 мл /мин =
= 1000 мл О2/мин.
^ Уравнение Фика выражает связь между потреблением O2, артериовенозной разницей по кислороду и сердечным выбросом:
Потребление O2 = VO2 = Qt x (CaO2 - CvO2). После преобразования получаем:
CaO2 - CvO2 = VO2XQt-
Следовательно, артериовенозную разницу можно рассматривать как меру адекватности доставки кислорода.
При нормальном потреблении кислорода около 250 мл/мин и сердечном выбросе 5000 мл/мин нормальная артериовенозная разница, согласно этому уравнению, составит 5 мл O2/!OO мл крови. Заметим, что при этом нормальный коэффициент экстракции O2 [(CaO2 - CvO2)/CaO2] составит 25 %, т. е. 5 мл/20 мл. Таким образом, в норме организм потребляет только 25 % кислорода, переносимого гемоглобином. Когда потребность в O2 превосходит возможность его доставки, то коэффициент экстракции становится выше 25 %. На-
оборот, если доставка O2 превышает потребность, то коэффициент экстракции падает ниже 25 %.
Если доставка кислорода снижена умеренно, потребление кислорода не изменяется благодаря увеличению экстракции O2 (насыщение гемоглобина кислородом в смешанной венозной крови снижается); в этом случае VO2 не зависит от доставки. По мере дальнейшего снижения DO2 достигается критическая точка, в которой VO2 становится прямо пропорционально DO2. Состояние, при котором потребление кислорода зависит от доставки, характеризуется прогрессирующим лак-тат-ацидозом (гл. 30), обусловленным клеточной гипоксией.
^ Кислородный резерв
Понятие кислородного резерва имеет большое значение в анестезиологии. Когда в результате апноэ прекращается поступление в организм кислорода, то в ходе клеточного метаболизма потребляется имеющийся кислородный резерв; после того как резерв исчерпан, развивается гипоксия и наступает смерть клеток. Теоретически нормальный кислородный резерв у взрослого человека составляет около 1500 мл. Он включает остатки кислорода в легких; кислород, находящийся в связи с гемоглобином и миоглобином; кислород, растворенный в жидкостях организма. К сожалению, высокое сродство гемоглобина к кислороду (сродство мио-глобина к кислороду еще выше), а также незначительное количество кислорода, физически растворенного в тканях, представляют собой очень малый резерв. Следовательно, основным источником кислорода является дыхательная смесь, находящаяся в легких в объеме, соответствующем ФОЕ (исходный объем при апноэ). Необходимо отметить, что только около 80 % этого объема может быть использовано.
При наступлении апноэ у больного, дышавшего перед этим атмосферным воздухом, в легких имеется примерно 480 мл кислорода (если FiO2 = 0,21 и ФОЕ = 2300 мл, то объем кислорода составит FiO2 X ФОЕ; 0,21 X 2300 мл = 480 мл). Метаболически активные ткани быстро используют этот резерв (предположительно со скоростью потребления кислорода); в течение 90 с развивается тяжелая гипоксемия. Возникновение гипоксемии можно отсрочить путем увеличения FiO2 перед апноэ. После дыхания чистым кислородом легкие содержат 2300 мл кислорода, что задерживат развитие гипоксемии после апноэ на 4-5 мин. Данная концепция лежит в основе проведения преоксигена-ции перед индукцией анестезии (гл. 5).
^ 2. УГЛЕКИСЛЫЙ ГАЗ
CO2 транспортируется кровью в физически растворенном виде, в составе бикарбоната и в комплексе с белками в виде карбаминовых соединений (табл. 22-6). Сумма всех трех форм составляет общее содержание CO2 в крови, которое стандартным образом измеряется при анализе электролитов.
^ Физически растворенный CO2
CO2 растворяется в крови лучше, чем кислород, коэффициент его растворимости 0,031 ммоль/л/ мм рт. ст. при 37 0C (0,067 мл/100 мл/мм рт. ст.)
Бикарбонат
В водных растворах CO2 медленно вступает в связь с водой, образуя бикарбонат:
H2O+ CO2-H++HCO3".
В плазме в эту реакцию вступает менее 1 % растворенного CO2, тогда как в эритроцитах и в эндо-телиальных клетках имеется фермент карбо-ангидраза, который ее ускоряет. В результате бикарбонат представляет самую большую фракцию CO2 в крови (табл. 22-6). Ацетазоламид, будучи ингибитором карбоангидразы, может нарушать доставку CO2 от тканей к альвеолам.
В венозных сегментах капилляров большого круга кровообращения CO2 поступает в эритроциты, где трансфомируется в бикарбонат, который диффундирует из эритроцитов в плазму. Для поддержания электрического равновесия из плазмы в эритроциты перемещаются ионы Cl". В легочных капиллярах происходит обратный процесс: ионы Cl" выходят из эритроцитов, а бикарбонат поступает в них для превращения в CO2, который диффундирует в альвеолы. Перемещение ионов
Cl" носит название хлоридного сдвига, или сдвига Гамбургера.
^ Карбаминовые соединения
CO2 может реагировать с аминогруппами белков согласно реакции:
R-NH2 + CO2 — RNH-CO2" + H+.
При физиологических значениях рН только небольшое количество CO2 переносится в этой форме, главным образом, в комплексе с гемоглобином (карбаминогемоглобин). Сродство дезоксигениро-ванного гемоглобина (дезоксигемоглобина) к CO2 в 3,5 раза выше, чем у оксигемоглобина. Увеличение сродства крови к CO2 при ее деоксигенации часто называют эффектом Холдейна (табл. 22-6). В норме PCO2 существенно не влияет на фракцию CO2, которая транспортируется в виде карбами-ногемоглобина.
^ Влияние гемоглобинового буфера на транспорт CO2
Эффект Холдейна отчасти обусловлен буферными свойствами гемоглобина (гл. 30). При нормальном рН гемоглобин может выполнять роль буфера за счет высокого содержания гистидина. Кроме того, кислотно-основные свойства гемоглобина зависят от степени его оксигенации:
H++HbO2-> HbH++O2.
После высвобождения кислорода в тканевых капиллярах молекула гемоглобина начинает вести себя подобно основанию; связывая ионы водорода, гемоглобин смещает равновесие СО2-бикарбонат преимущественно в сторону образования бикарбоната:
CO2 + H2O + HbO2 — HbH++ HCO3"+ O2.
^ ТАБЛИЦА 22-6. Транспорт СО2(из расчета на 1 л цельной крови)
| Форма | Плазма | Эритроциты | Плазма + эритроциты | Доля (%) |
| Цельная смешанная венозная кровь | ||||
| Растворенный CO2 | 0,76 | 0,51 | 1,27 | 5,5 |
| Бикарбонат | 14,41 | 5,92 | 20,33 | 87,2 |
| Карбаминовые соединения | Незначительное | 1,70 | 1,70 | 7,3 |
| Общее содержание CO2 (ммоль/л) | 15,17 | 8,13 | 23,30 | |
| Цельная артериальная кровь | | | | |
| Растворенный CO2 | 0,66 | 0,44 | 1,10 | 5,1 |
| Бикарбонат | 13,42 | 5,88 | 19,30 | 89,8 |
| Карбаминовые соединения | Незначительное | 1,10 | 1,10 | 5,1 |
| Общее содержание CO2 (ммоль/л) | 14,08 | 7,42 | 21,50 | |
Если не указано иное, значения везде выражены в ммоль. (С разрешения. Из: Nunn J. R ^ Applied Respiratory Physiology, 4th ed. Butterworths, 1993.)
В результате дезоксигемоглобин увеличивает количество CO2, переносимого венозной кровью в форме бикарбоната. По мере того как CO2 поступает из тканей и превращается в бикарбонат, общее содержание CO2 в крови растет (табл. 22-6). В легких процесс имеет противоположное направление. Оксигенация гемоглобина усиливает его кислотные свойства, и высвобождение ионов водорода смещает равновесие преимущественно в сторону образования CO2:
O2 + HCO3" + HbH+-CO2 + H2O + HbO2.
Концентрация бикарбоната снижается по мере того, как образуется и элиминируется CO2, так что в легких падает общее содержание CO2 в крови. Отметим, что имеется разница в содержании CO2 в цельной крови (табл. 22-6) и плазме (табл. 22-7).
Кривая диссоциации CO2
Кривую диссоциации CO2 можно построить в виде графического отображения зависимости общего содержания CO2 от PCO2. Аналогично можно количественно отобразить долю каждой из форм CO2 (рис. 22-24).
Запасы CO2
Запасы углекислого газа в организме велики (приблизительно 120 л у взрослого человека) и представлены главным образом в виде растворенного CO2 и бикарбоната. Когда равновесие между выработкой и элиминаций углекислого газа нарушается, то в течение 20-30 мин устанавливается новое равновесие (для кислорода такое уравновешивание происходит не позднее 4-5 мин). По скорости уравновешивания запасы CO2 подразделяют на быстрые, средние и медленные. Емкости средних и медленных запасов больше, а это значит, что при резких изменениях вентиляции скорость увеличения PaCO2 меньше, чем скорость снижения.
Регуляция дыхания
Автоматизм самостоятельного дыхания является результатом ритмической активности дыхатель-
ных центров в стволе головного мозга. Дыхательные центры управляют дыхательными мышцами, что позволяет поддерживать нормальное напряжение O2 и CO2 в организме. Базальная активность нервных центров модулируется сигналами из других областей головного мозга, произвольными и непроизвольными, а также центральными и периферическими рецепторами.
